 ピートル
ピートル
製品の特性
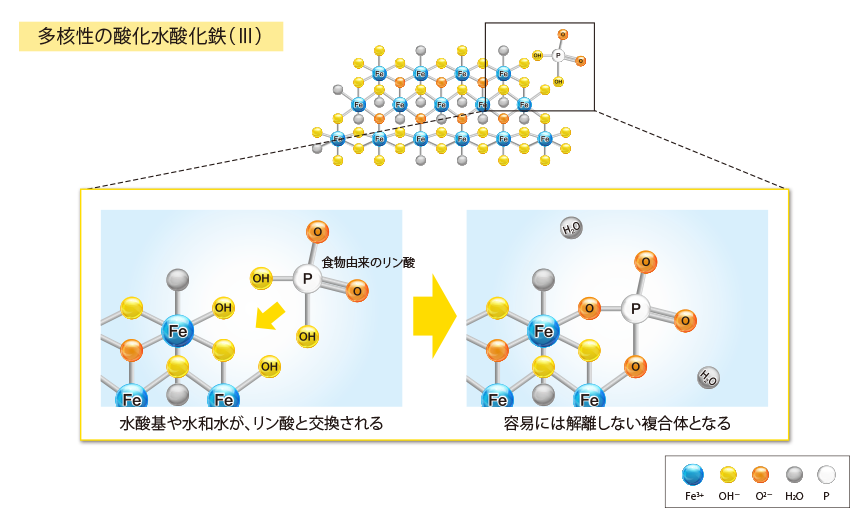
鉄(Ⅲ)複合体構造のリン吸着薬1-3)
ピートルは、生理的な金属である鉄(Ⅲ)を含有した、独自の複合体構造を有するリン吸着薬です。
スクロオキシ水酸化鉄は、消化管内でスクロースとデンプンが消化された後、多核性の酸化水酸化鉄(Ⅲ)の配位子(水酸基および水和水)とリン酸が結合し、消化管からのリン吸収を抑制することにより、血清リン濃度低下作用を示します。
1)Geisser P, et al.: Clin Nephrol. 2010; 74: 4-11.(本試験はVifor Pharma社の資金提供により実施された)
2)Sprague SM, et al.: Clin Investig (Lond). 2015; 5: 9-21.(本試験はVifor Pharma社の資金提供により実施された)
3)Wilhelm M, et al.: Clin Nephrol. 2014; 81: 251-258.(本論文の著者はVifor Pharma社の社員である)
2)Sprague SM, et al.: Clin Investig (Lond). 2015; 5: 9-21.(本試験はVifor Pharma社の資金提供により実施された)
3)Wilhelm M, et al.: Clin Nephrol. 2014; 81: 251-258.(本論文の著者はVifor Pharma社の社員である)
第Ⅱ相臨床試験:主要評価項目1,2)
1)承認時評価資料:血液透析患者を対象とした第Ⅱ相臨床試験
2)Koiwa F, et al.: Clin Exp Nephrol. 2017; 21: 513-522.(本試験はキッセイ薬品工業株式会社の支援により実施された)
2)Koiwa F, et al.: Clin Exp Nephrol. 2017; 21: 513-522.(本試験はキッセイ薬品工業株式会社の支援により実施された)
(一部用法・用量で定められた開始用量外の成績が含まれるが、承認時に評価されたデータのため掲載する。)
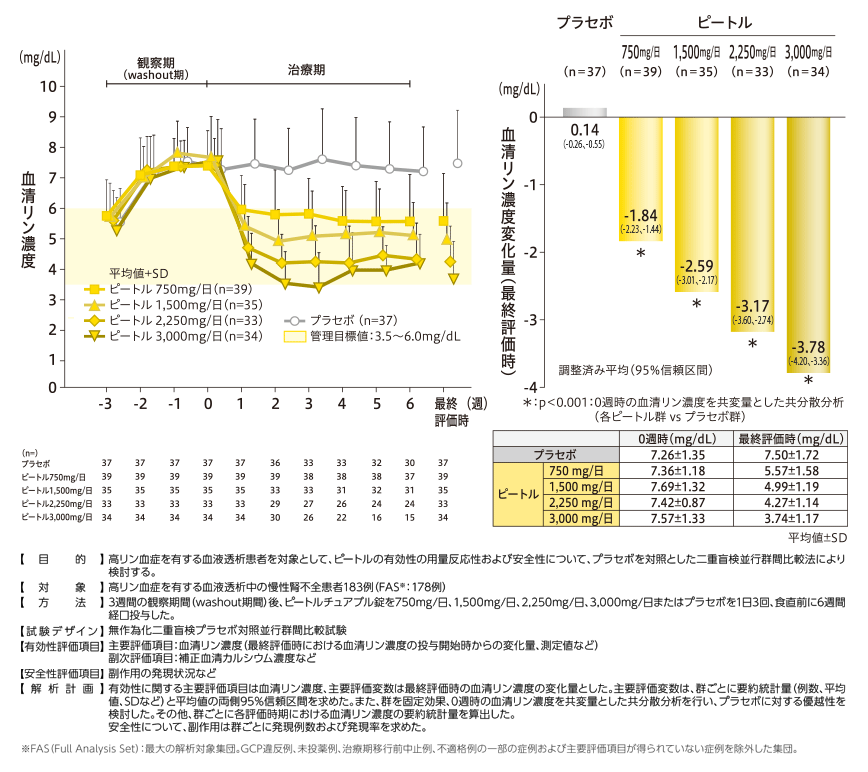
- 6.用法及び用量 通常、成人には、鉄として1回250mgを開始用量とし、1日3回食直前に経口投与する。以後、症状、血清リン濃度の程度により適宜増減するが、最高用量は1日3000mgとする。
- 7.用法及び用量に関連する注意(抜粋)
- 7.2増量を行う場合は、増量幅を鉄として1日あたりの用量で750mgまでとし、1週間以上の間隔をあけて行うこと。
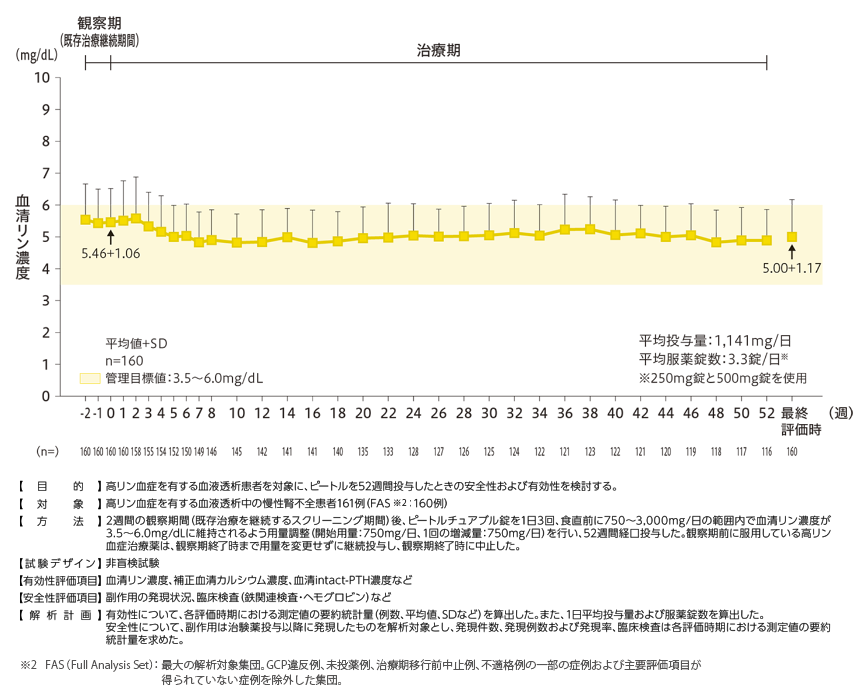
52週間のリン濃度管理(長期投与試験)1,2)
1)承認時評価資料:血液透析患者を対象とした長期投与試験
2)Koiwa F, et al.: J Ren Nutr. 2017; 27: 346-354.(本試験はキッセイ薬品工業株式会社の支援により実施された)
2)Koiwa F, et al.: J Ren Nutr. 2017; 27: 346-354.(本試験はキッセイ薬品工業株式会社の支援により実施された)
ピートル投与後、52週間、血清リン濃度は管理目標値(3.5~6.0mg/dL)※の範囲内に維持されました。
※慢性腎臓病に伴う骨・ミネラル代謝異常(CKD-MBD)の診療ガイドライン3)の管理目標値
3)日本透析医学会: 透析会誌. 2012; 45: 301-356.
3)日本透析医学会: 透析会誌. 2012; 45: 301-356.
- 7.用法及び用量に関連する注意(抜粋)
- 7.2増量を行う場合は、増量幅を鉄として1日あたりの用量で750mgまでとし、1週間以上の間隔をあけて行うこと。
- 8. 重要な基本的注意(抜粋)
- 8.1本剤は、定期的に血清リン、血清カルシウム及び血清PTH濃度を測定しながら投与すること。血清リン、血清カルシウム及び血清PTH濃度の管理目標値及び測定頻度は、学会のガイドライン等、最新の情報を参考にすること。低カルシウム血症の発現あるいは悪化がみられた場合には、活性型ビタミンD製剤やカルシウム製剤の投与を考慮し、カルシウム受容体作動薬が使用されている場合には、カルシウム受容体作動薬の減量等も考慮すること。また、二次性副甲状腺機能亢進症の発現あるいは悪化がみられた場合には、活性型ビタミンD製剤、カルシウム製剤、カルシウム受容体作動薬の投与あるいは他の適切な治療法を考慮すること。
ドーナツ型のチュアブル錠
ピートルチュアブル錠は、水なしでも服用できるドーナツ型の製剤です。
ピートルチュアブル錠の形状


崩壊性(in vitro)
ピートルの崩壊時間は11~16分でした。1)

| 250mg | |||||
|---|---|---|---|---|---|
| ロット | 平均崩壊時間[最小-最大](分) | ||||
| ピートル チュアブル錠 |
ピートル 顆粒分包※ |
||||
| pH1.2液 | pH4.0液 | pH6.8液 | 水 | 水 | |
| ロット1 | 15[13-16] | 13[12-14] | 14[12-14] | 14[13-14] | 14[13-15] |
| ロット2 | 13[13-14] | 12[11-12] | 12[12-13] | 13[13-13] | 13[13-13] |
| ロット3 | 14[12-14] | 12[11-14] | 12[11-13] | 13[13-14] | 14[13-14] |
| 500mg | |||||
|---|---|---|---|---|---|
| ロット | 平均崩壊時間[最小-最大](分) | ||||
| ピートル チュアブル錠 |
ピートル 顆粒分包※ |
||||
| pH1.2液 | pH4.0液 | pH6.8液 | 水 | 水 | |
| ロット1 | 16[15-16] | 13[12-14] | 14[13-14] | 14[14-15] | 14[13-15] |
| ロット2 | 15[13-16] | 12[11-13] | 13[13-14] | 14[14-15] | 13[13-13] |
| ロット3 | 16[15-16] | 12[12-13] | 14[13-16] | 15[13-16] | 14[13-14] |
※ピートル顆粒分包は同一のバルク製剤を用い、包装質量を調整して顆粒分包250mgおよび500mgとするため、ピートル顆粒分包250mgおよび500mgの崩壊時間(実測値)は同一である。
- 方法
-
第十六改正日本薬局方 一般試験法 崩壊試験法に従った。試験液は以下の通り。
pH1.2液:日局溶出試験第1液、pH4.0液:薄めたMcIlvaine緩衝液、pH6.8液:日局溶出試験第2液
1)承認時評価資料:in vitro崩壊性試験
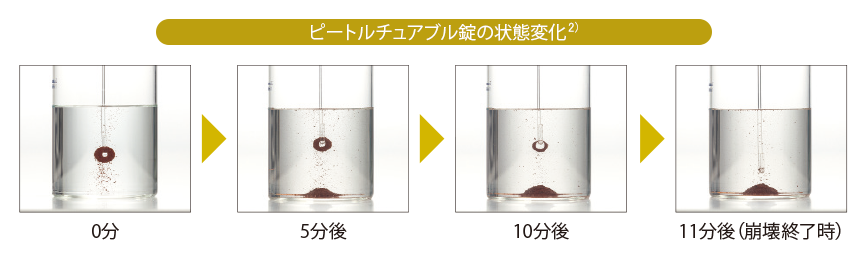
- 方法
-
第十六改正日本薬局方 一般試験法に定める崩壊試験法を応用し、ピートルチュアブル錠250mgの崩壊挙動の観察を行った。
試験液:pH4.0(水に塩酸を希釈して調整)、37℃
2)社内資料:崩壊試験
マイクロタブレット型の顆粒剤
ピートル顆粒分包は、かまずに服用できるマイクロタブレット型の顆粒剤です。
ピートル顆粒分包の形状

崩壊性(in vitro)
ピートルの崩壊時間は11~16分でした。1)

| 250mg | |||||
|---|---|---|---|---|---|
| ロット | 平均崩壊時間[最小-最大](分) | ||||
| ピートル チュアブル錠 |
ピートル 顆粒分包※ |
||||
| pH1.2液 | pH4.0液 | pH6.8液 | 水 | 水 | |
| ロット1 | 15[13-16] | 13[12-14] | 14[12-14] | 14[13-14] | 14[13-15] |
| ロット2 | 13[13-14] | 12[11-12] | 12[12-13] | 13[13-13] | 13[13-13] |
| ロット3 | 14[12-14] | 12[11-14] | 12[11-13] | 13[13-14] | 14[13-14] |
| 500mg | |||||
|---|---|---|---|---|---|
| ロット | 平均崩壊時間[最小-最大](分) | ||||
| ピートル チュアブル錠 |
ピートル 顆粒分包※ |
||||
| pH1.2液 | pH4.0液 | pH6.8液 | 水 | 水 | |
| ロット1 | 16[15-16] | 13[12-14] | 14[13-14] | 14[14-15] | 14[13-15] |
| ロット2 | 15[13-16] | 12[11-13] | 13[13-14] | 14[14-15] | 13[13-13] |
| ロット3 | 16[15-16] | 12[12-13] | 14[13-16] | 15[13-16] | 14[13-14] |
※ピートル顆粒分包は同一のバルク製剤を用い、包装質量を調整して顆粒分包250mgおよび500mgとするため、ピートル顆粒分包250mgおよび500mgの崩壊時間(実測値)は同一である。
- 方法
-
第十六改正日本薬局方 一般試験法 崩壊試験法に従った。試験液は以下の通り。
pH1.2液:日局溶出試験第1液、pH4.0液:薄めたMcIlvaine緩衝液、pH6.8液:日局溶出試験第2液
1)承認時評価資料:in vitro崩壊性試験
副作用(チュアブル錠承認時)1)
ピートル投与による副作用は494例中159例(32.2%)に認められました。
その主な副作用は下痢(22.7%)でした(チュアブル錠承認時)。
添付文書の副作用の項および臨床成績の項の安全性の結果をご参照ください。
1)承認時評価資料





