腹膜透析患者第Ⅲ相臨床試験1)
1)承認時評価資料:腹膜透析患者を対象とした第Ⅲ相臨床試験
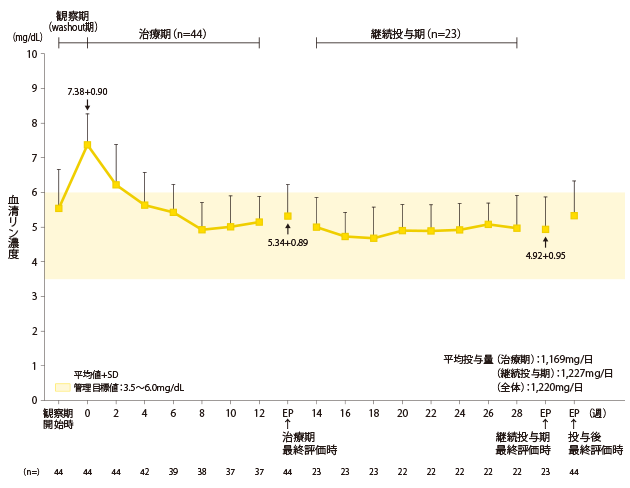
血清リン濃度の推移
0週時7.38±0.90mg/dLであった血清リン濃度は、治療期最終評価時に5.34±0.89mg/dL、28週までの継続投与期最終評価時には4.92±0.95mg/dLでした。
【試験概要】
- 目的
- 高リン血症を有する腹膜透析患者を対象にピートルを12週間投与したときの有効性および安全性を検討する(治療期)。また、継続投与の基準を満たす患者については28週まで継続投与したときの安全性および有効性を確認する(継続投与期)。
- 対象
- 高リン血症を有する腹膜透析中の慢性腎不全患者44例(FAS※:44例)
- 方法
-
2~4週間の観察期間(washout期間)後、ピートルチュアブル錠を1日3回、食直前に750~3,000mg/日の範囲内で血清リン濃度が3.5~6.0mg/dLに維持されるよう用量調整(開始用量:750mg/日、1回の増減量:750mg/日)を行い、12週間経口投与した。
投与12週来院時までに継続投与期移行基準を満たす患者には、継続してピートルを28週まで経口投与した。(継続投与期移行基準:コンプライアンスが良好で、継続投与に問題がない患者) - 試験デザイン
- 非盲検試験
- 有効性評価項目
- 血清リン濃度、補正血清カルシウム濃度、血清intact-PTH濃度など
- 安全性評価項目
- 副作用の発現状況など
- 解析計画
-
有効性について、各評価時期における測定値の要約統計量(例数、平均値、SDなど)を算出した。また、治療期および継続投与期を含む治療期・継続投与期全体の1日平均投与量を算出した。
安全性について、副作用は治験薬投与以降に発現したものを解析対象とし、治療期および継続投与期を含む治療期・継続投与期全体の発現件数、発現例数および発現率を求めた。
| ※FAS(Full Analysis Set) : | 最大の解析対象集団。GCP違反例、未投薬例、治療期移行前中止例、不適格例の一部の症例および主要評価項目が得られていない症例を除外した集団。 |
- 7.用法及び用量に関連する注意(抜粋)
- 7.2増量を行う場合は、増量幅を鉄として1日あたりの用量で750mgまでとし、1週間以上の間隔をあけて行うこと。
- 8.重要な基本的注意(抜粋)
- 8.1本剤は、定期的に血清リン、血清カルシウム及び血清PTH濃度を測定しながら投与すること。血清リン、血清カルシウム及び血清PTH濃度の管理目標値及び測定頻度は、学会のガイドライン等、最新の情報を参考にすること。低カルシウム血症の発現あるいは悪化がみられた場合には、活性型ビタミンD製剤やカルシウム製剤の投与を考慮し、カルシウム受容体作動薬が使用されている場合には、カルシウム受容体作動薬の減量等も考慮すること。また、二次性副甲状腺機能亢進症の発現あるいは悪化がみられた場合には、活性型ビタミンD製剤、カルシウム製剤、カルシウム受容体作動薬の投与あるいは他の適切な治療法を考慮すること。