国内第Ⅲ相臨床試験(KLH2302)1)
有効性
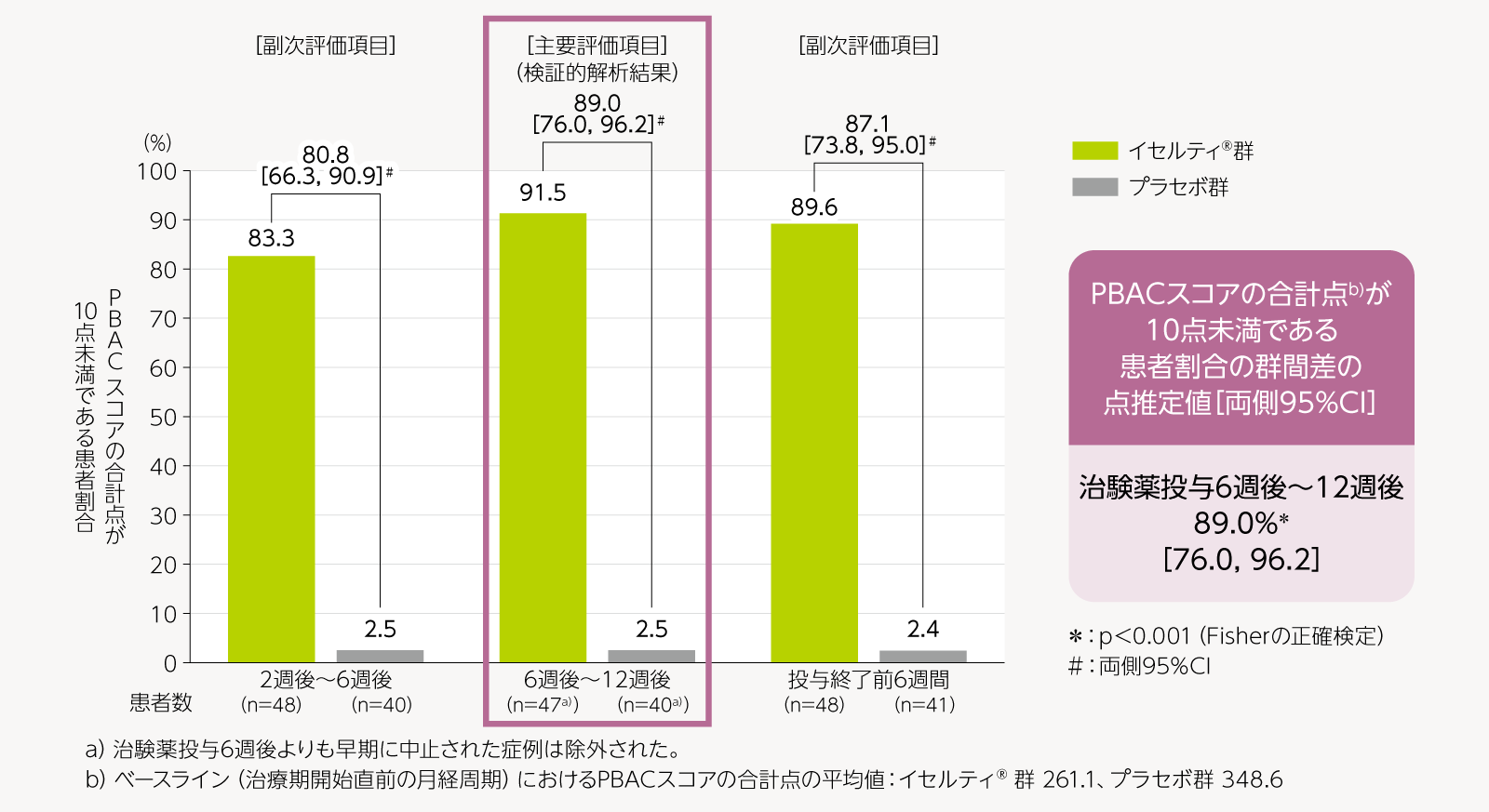
- 治験薬投与6週後から12週後までのPBACスコアの合計点が10点未満である患者割合[主要評価項目(検証的解析結果)]
治験薬投与2週後から6週後まで、投与終了前6週間のPBACスコアの合計点が10点未満である患者割合[副次評価項目] -
主要評価項目である治験薬投与6週後から12週後までのPBACスコアの合計点が10点未満である患者割合は、イセルティ®群がプラセボ群と比較して有意に高かった(Fisher の正確検定、p<0.001)。
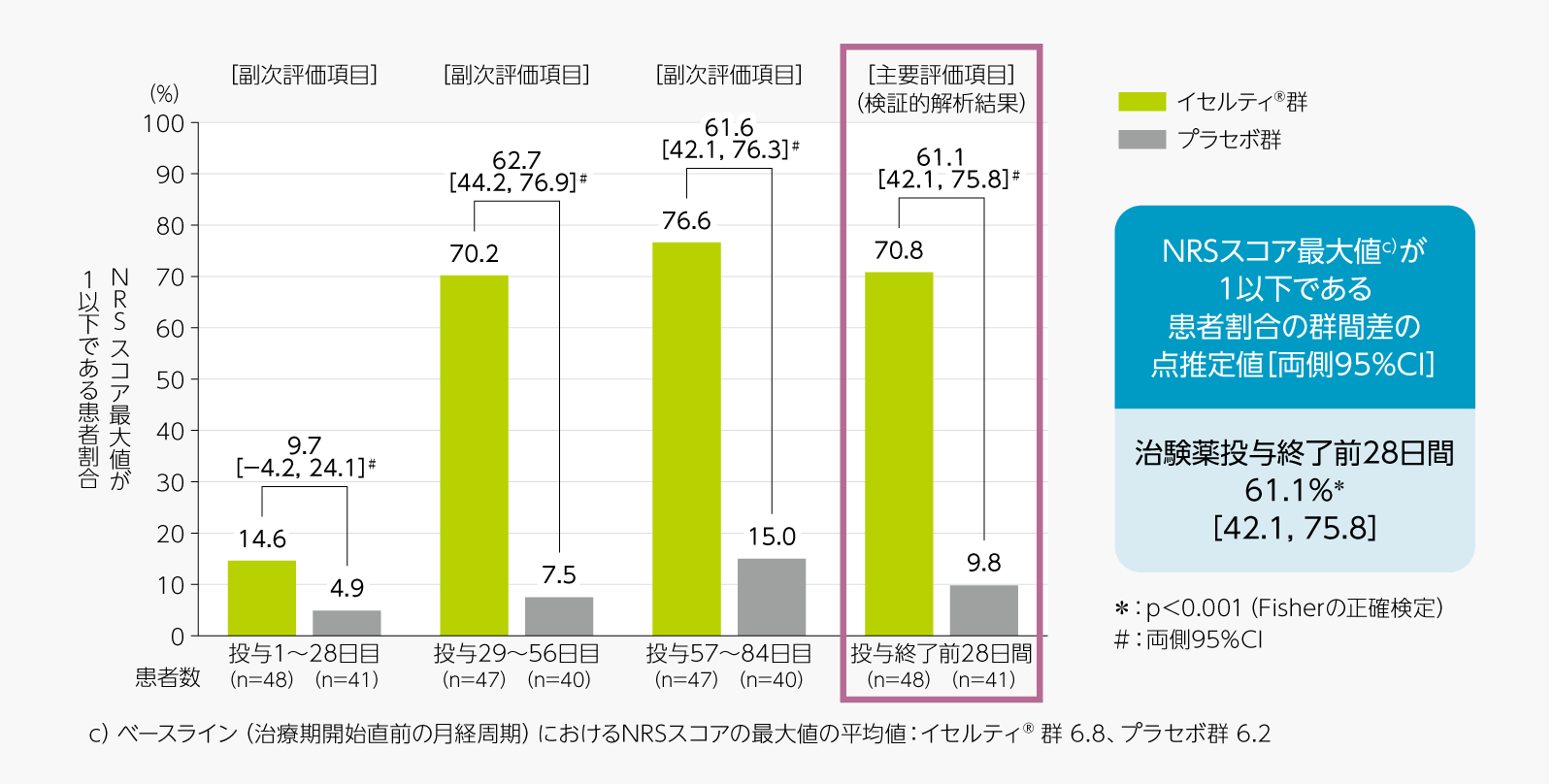
- 治験薬投与終了前28日間における疼痛症状に対するNRSスコア最大値が1以下である患者割合[主要評価項目(検証的解析結果)]
治験薬投与1日目~28日目まで、29日目~56日目まで、57日目~84日目までにおける疼痛症状に対するNRSスコア最大値が1以下である患者割合[副次評価項目] -
主要評価項目である治験薬投与終了前28日間における疼痛症状に対するNRSスコア最大値が1以下である患者割合は、イセルティ®群がプラセボ群と比較して有意に高かった(Fisher の正確検定、p<0.001)。
上記の結果より、過多月経及び疼痛症状に関する2つの主要評価項目において、いずれもイセルティ®群がプラセボ群よりも有意に高いことが検証されたため、プラセボに対する優越性が検証された。
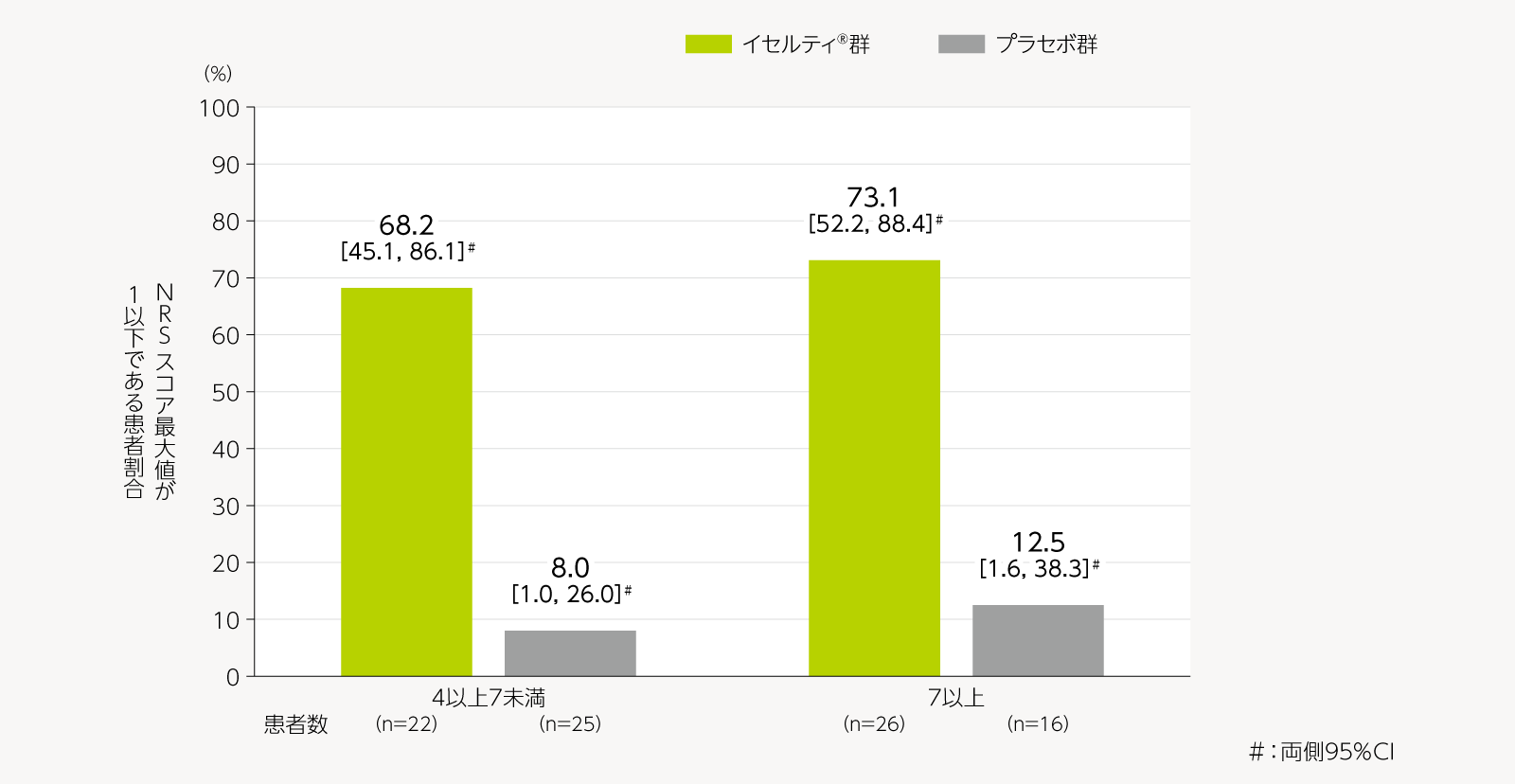
- 疼痛症状に関する主要評価項目のサブグループ解析(ベースラインのNRSスコア最大値4以上7未満/7以上の部分集団)
-
ベースラインのNRSスコア最大値(4以上7未満/7以上)ごとの治験薬投与終了前28日間におけるNRSスコア最大値1以下である患者割合及びその両側95%CIは以下のとおりであった。
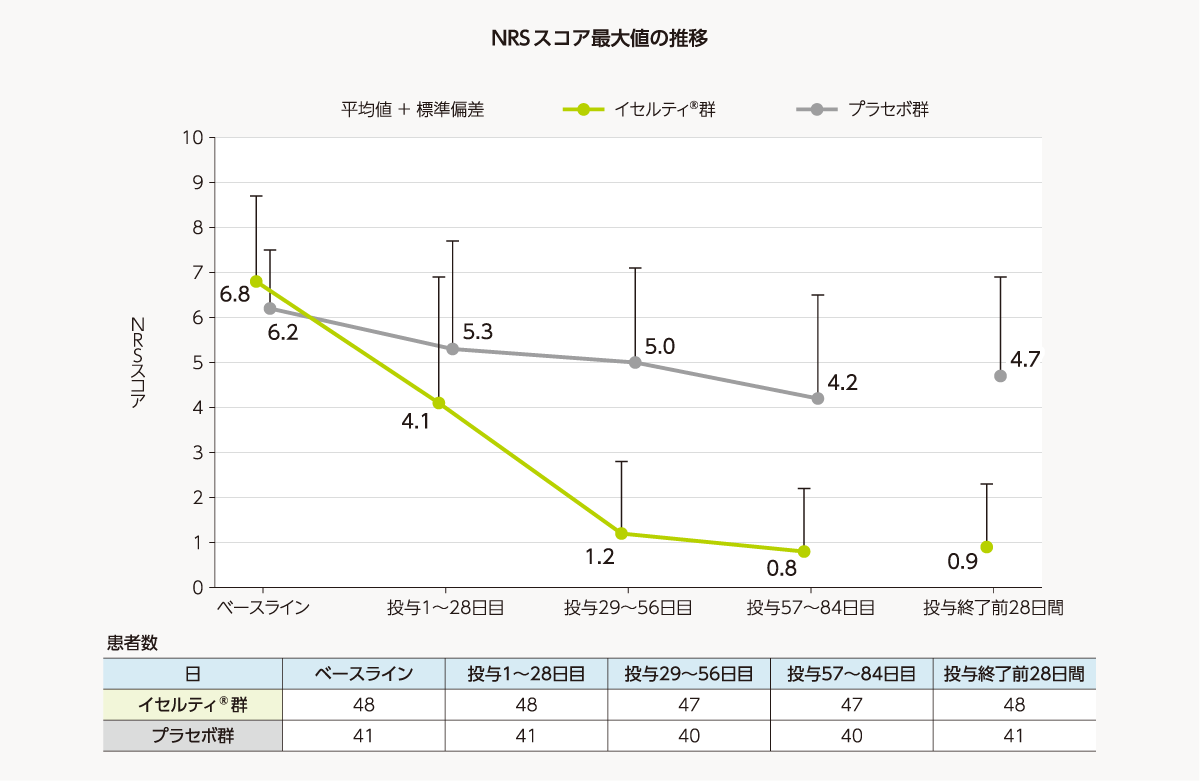
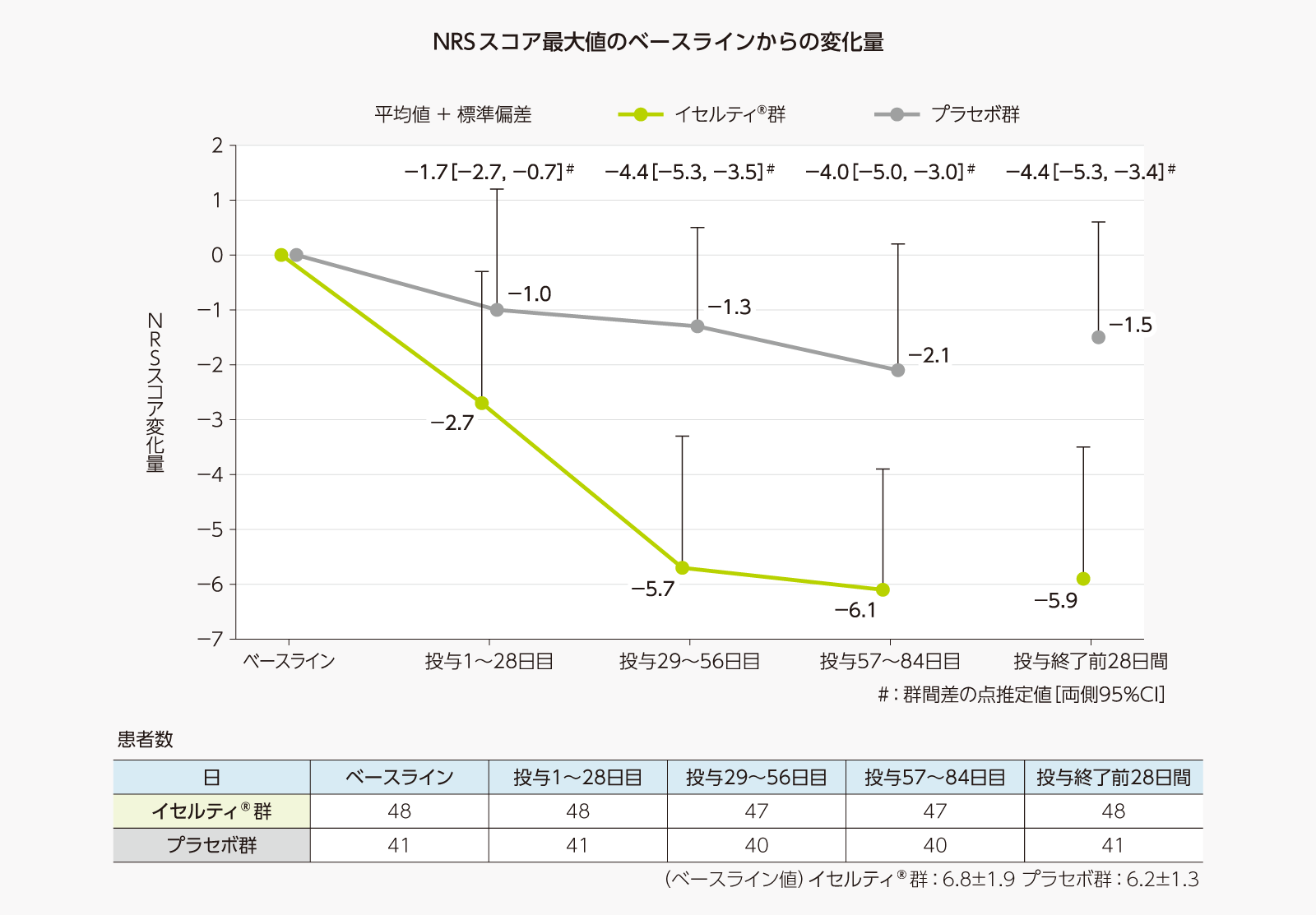
- NRSスコア最大値の推移及びベースラインからの変化量[副次評価項目]
-
NRSスコア最大値の推移及びベースラインからの変化量は、以下のとおりであった。
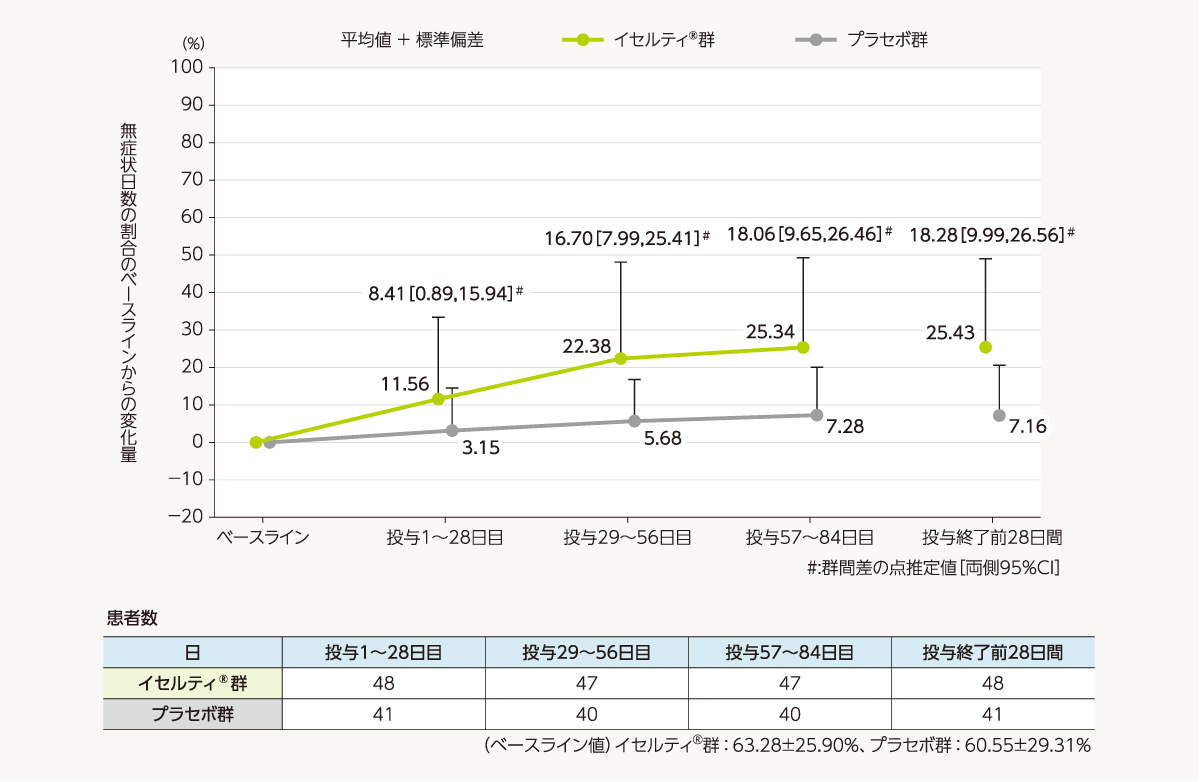
- 無症状日数(疼痛症状に対するNRSスコア0の日数)の割合のベースラインからの変化量[副次評価項目]
-
無症状日数の割合のベースラインからの変化量は、以下のとおりであった。
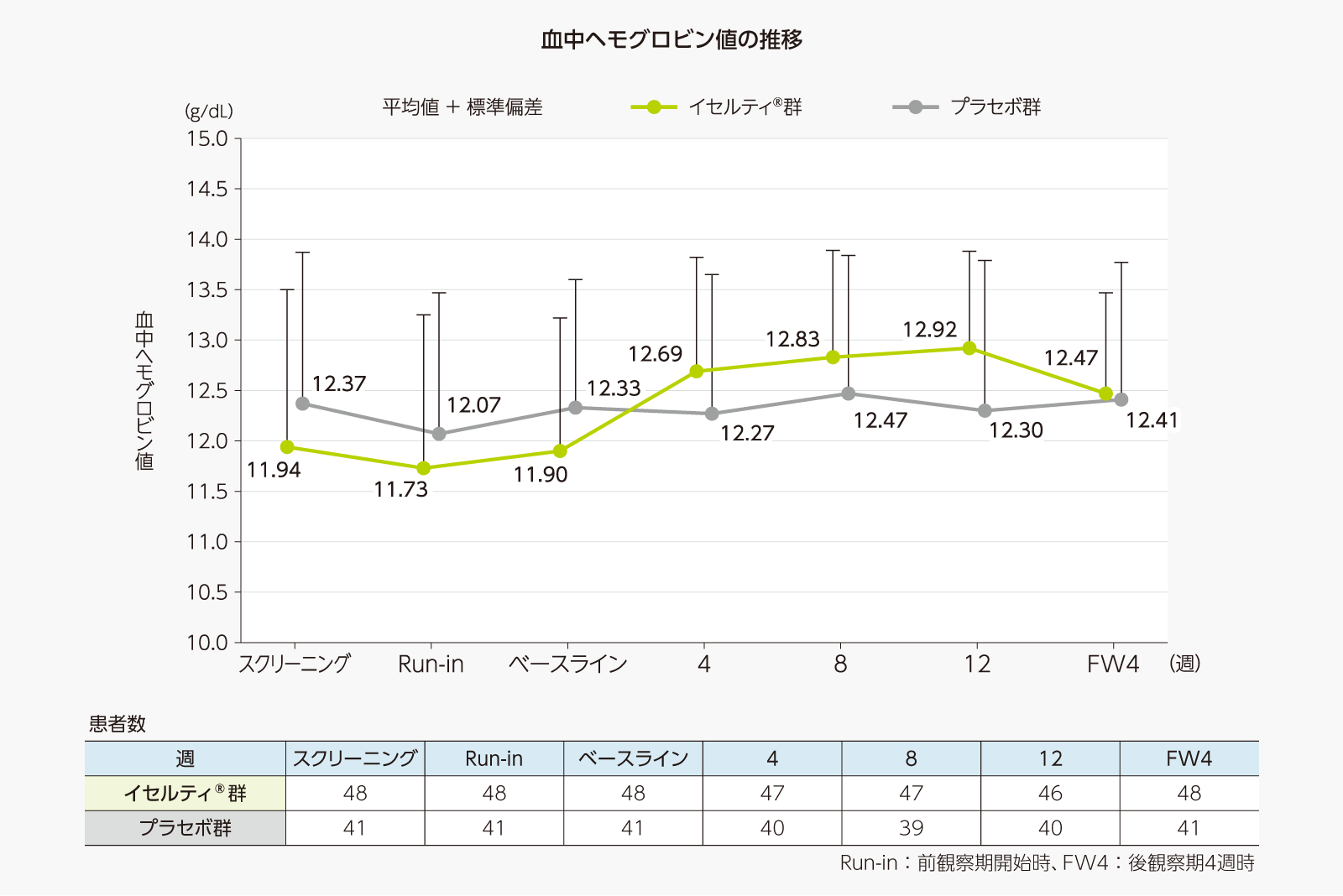
- 血中ヘモグロビン値の推移及びベースラインからの変化量[副次評価項目]
-
血中ヘモグロビン値の推移及びベースラインからの変化量は、以下のとおりであった。
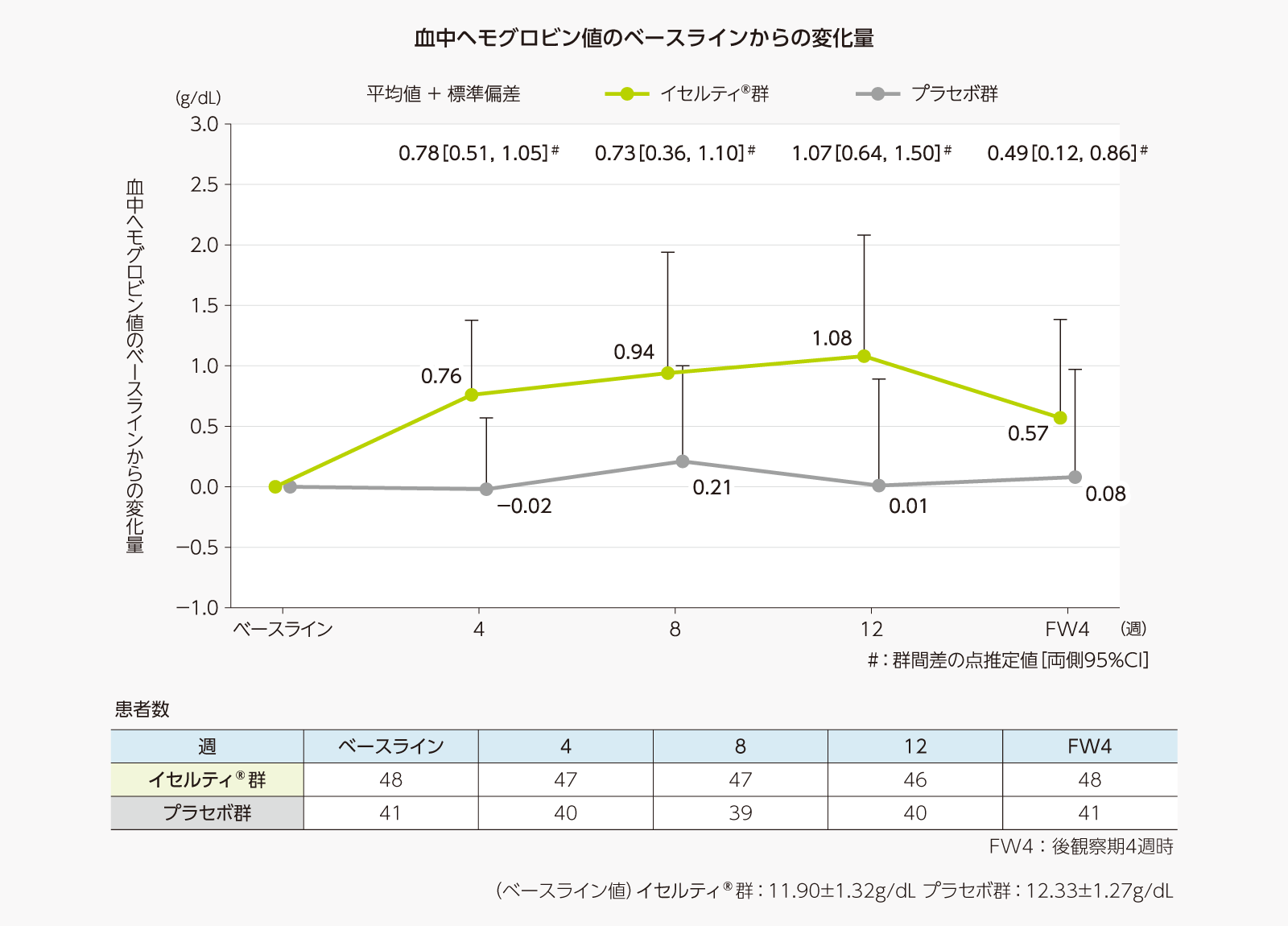
- 血中ヘモグロビン値に関する副次評価項目のサブグループ解析
(ベースラインの血中ヘモグロビン値が12g/dL未満の部分集団) -
血中ヘモグロビン値の推移及びベースラインからの変化量は、以下のとおりであった。
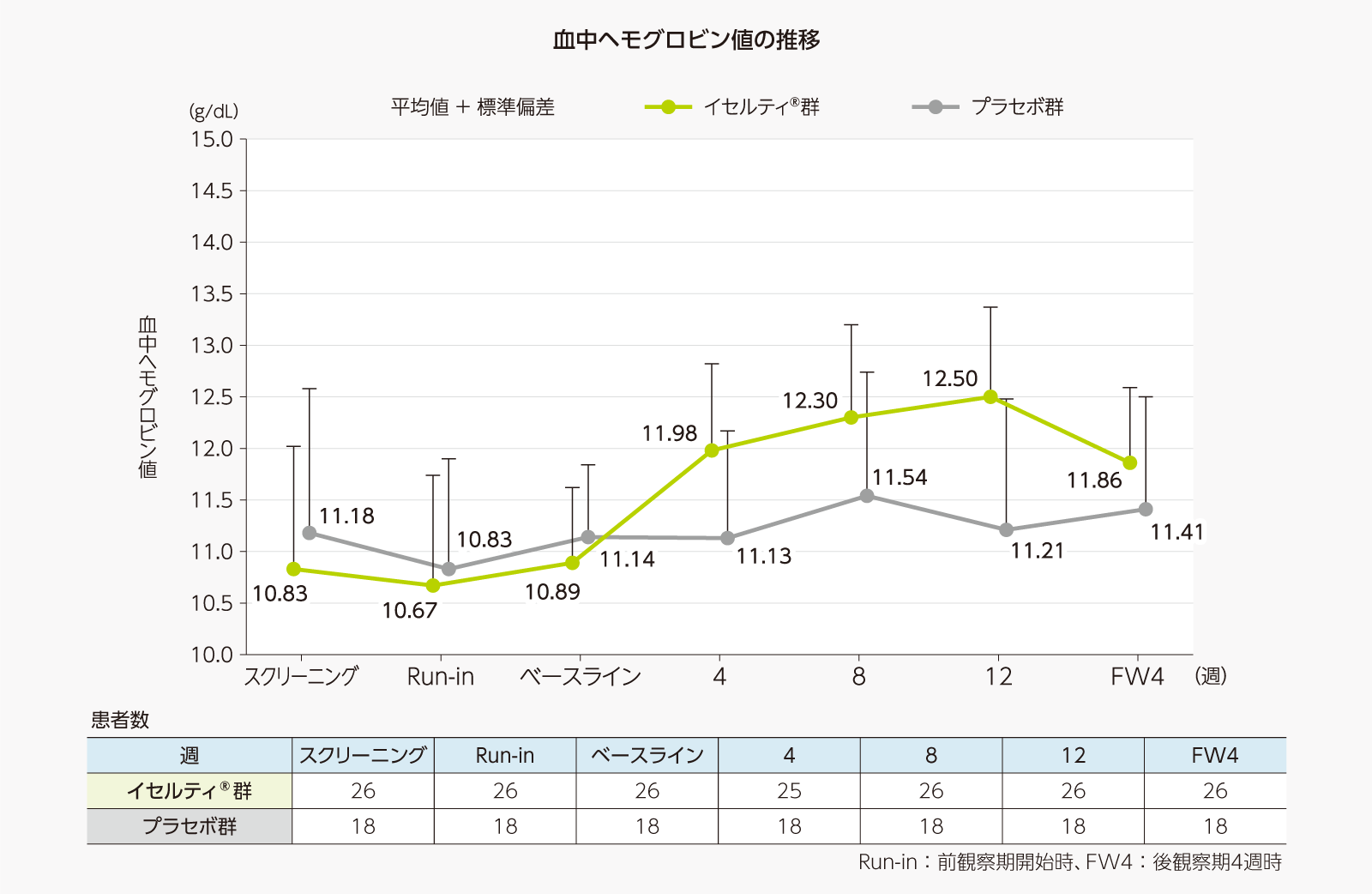

- UFS-QOLスコアのベースラインからの変化量[副次評価項目]
-
治験薬投与12週時及び治療期最終評価時のベースラインからの症状の重症度(Symptom Severity)及び健康に関するQOL(HRQL Total)スコアの変化量は、以下のとおりであった。
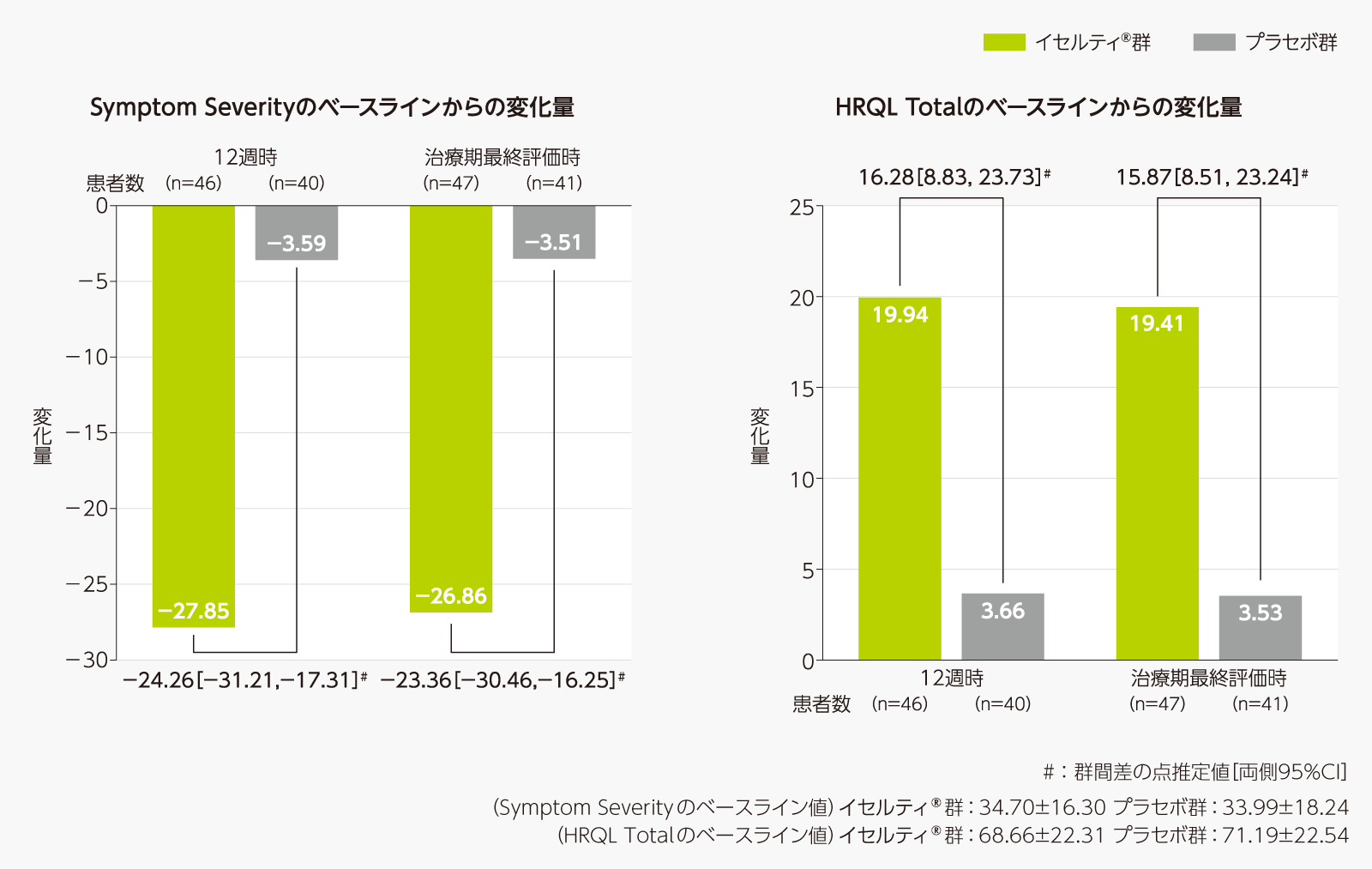
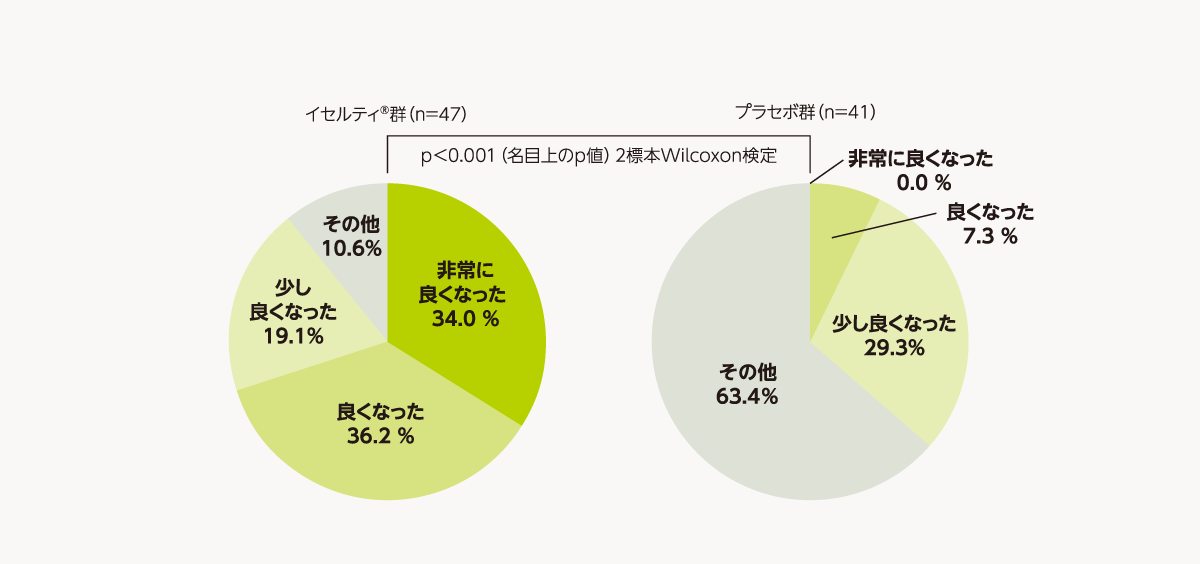
- 治療期最終評価時のPGICの全般的症状の割合[副次評価項目]
-
治療期最終評価時の全般的症状をPGICで評価した結果、以下のとおりであった。全般的症状はプラセボ群と比較してイセルティ®群で有意に改善した[2標本Wilcoxon 検定、p<0.001(名目上のp 値)]。