国内第Ⅲ相臨床試験(KLH2301)1)
目的
過多月経を有する子宮筋腫患者を対象として、イセルティ®200mgを1日1回12週間経口投与したときの過多月経に対する有効性について、リュープロレリン酢酸塩に対する非劣性を二重盲検法により検証する。
試験デザイン
実薬を対照とした多施設共同無作為化二重盲検並行群間比較試験
対象
20歳以上の閉経前子宮筋腫患者287例(イセルティ®群143例、リュープロレリン酢酸塩群144例)
主な選択基準
- 経腟超音波、腹部超音波、MRI、CT、腹腔鏡検査のいずれかによって子宮筋腫と診断されている患者
- スクリーニング期開始時・治療期開始時の経腟超音波検査で、以下の条件をすべて満たす筋腫核を1つ以上有していると確認された患者
最長径が3cm以上、石灰化を伴っていない、外科的治療を受けていない - 治療期開始直前の月経周期1回分のPBACスコアの合計点が120点以上で、過多月経と診断された患者
- スクリーニング期開始直前・前観察期開始直前・治療期開始直前に正常な月経周期(25~38日)を認め、かつ3日以上の連続的な出血を伴う月経が当該月経周期中に確認されている患者
方法
試験は、スクリーニング期、単盲検下でプラセボを投与する前観察期、二重盲検下で治験薬を投与する治療期24週間及び後観察期24週間で構成された。
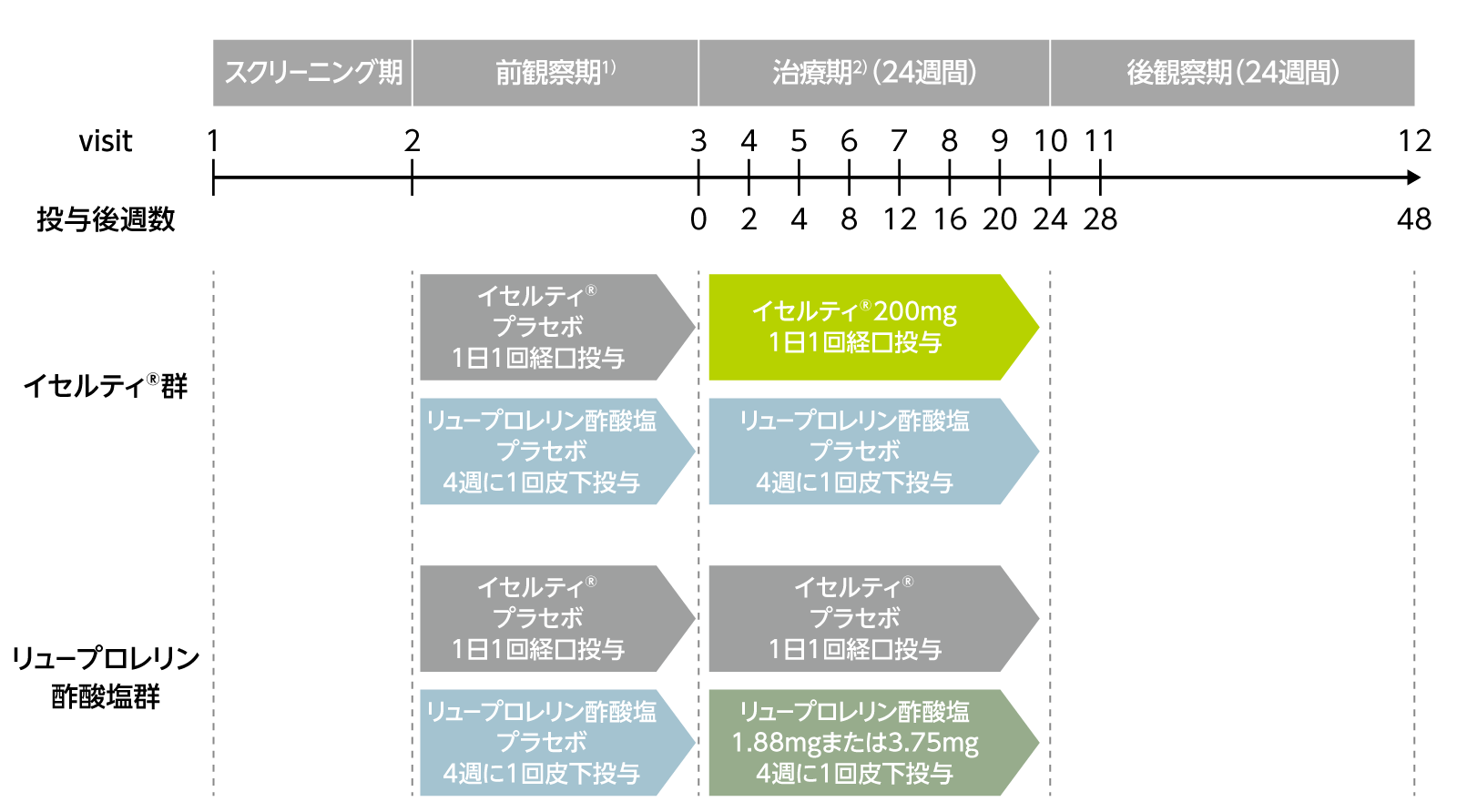
1)スクリーニング期開始後1回目の月経開始1〜5日目の来院を前観察期開始時とする。ただし、前観察期開始時の選択基準を満たしているもののスクリーニング期開始後1回目の月経開始1〜5日目に来院できない場合は、2回目の月経開始1〜5日目の来院を前観察期開始時とすることも可とする。
2)スクリーニング期開始後2回目の月経開始1〜5日目の来院を治療期開始時とする。ただし、スクリーニング期開始後2回目の月経開始1〜5日目に前観察期を開始した場合は、3回目の月経開始1〜5日目の来院を治療期開始時とする。
イセルティ®群では治験薬投与終了日+7日以内、リュープロレリン酢酸塩群では治験薬投与終了日+42日以内に実施された観察・検査項目のうち、規定の来院で最も遅い時点のデータを治療期最終評価時データとする。
- イセルティ®群:前観察期はそれぞれのプラセボを、治療期はイセルティ®200mgを1日1回経口投与、リュープロレリン酢酸塩のプラセボを4週に1回皮下投与する。
初回投与は月経1~5日目に実施する。
- リュープロレリン酢酸塩群:前観察期はそれぞれのプラセボを、治療期はイセルティ®のプラセボを1日1回経口投与、リュープロレリン酢酸塩1.88mg又は3.75mg注)を4週に1回皮下投与する。初回投与は月経1~5日目に実施する。
評価項目
有効性評価項目
主要評価項目
- 治験薬投与6週後から12週後までのPictorial Blood Loss Assessment Chart(PBAC)スコア*1の合計点が10点未満である患者割合(検証的解析項目)
副次評価項目
- PBACスコアの合計点が10点未満である患者割合(治験薬投与2週後から6週後まで、18週後から24週後まで、投与終了前6週間)及びそれまでの期間
- 無月経状態(PBACスコアの合計点が0点)までの期間
- 評価時点ごとの血中ヘモグロビン値の推移、血中ヘモグロビン値が12g/dL以上であった患者割合、筋腫核体積§及び子宮体積§のベースラインからの変化率 など
有効性に関するサブグループ解析
- 主要評価項目(治験薬投与6週後から12週後までのPBACスコアの合計点が10点未満である患者割合)におけるベースラインのPBACスコアの合計点が200点未満/200点以上の部分集団ごとの改善例の割合
- ベースラインの血中ヘモグロビン値が12g/dL未満の部分集団における血中ヘモグロビン値の推移及び血中ヘモグロビン値が12g/dL以上となった患者割合
安全性評価項目
副作用の発現割合、骨密度のベースラインからの変化率、治験薬最終投与から月経回復までの期間 など
解析計画
有効性評価項目
主要評価項目
治験薬投与6週後から12週後までのPBACスコアの合計点が10点未満である患者(改善例)割合
- 群ごとに改善例の例数及び割合とその両側95%信頼区間(CI)を示し、改善例の割合を図示した。イセルティ®群とリュープロレリン酢酸塩群の群間差(イセルティ®群−リュープロレリン酢酸塩群)の点推定値及びその両側95%CIを示した。
- 有意水準を片側2.5%、非劣性マージン−15%とし、Farrington-Manning法を用いてイセルティ®群とリュープロレリン酢酸塩群の非劣性検定を行い、両側95%CIの下限が非劣性マージン(-15%)以上であった場合に、リュープロレリン酢酸塩群に対するイセルティ®群の非劣性が検証されたものとした。(検証的解析項目)
副次評価項目
- 治験薬投与2週後から6週後まで、18週後から24週後まで、治験薬投与終了前6週間のPBACスコアの合計点が10点未満である患者割合は、群間差(イセルティ®群−リュープロレリン酢酸塩群)の点推定値及びその両側95%CIを示した。
- PBACスコアの合計点が10点未満となるまでの期間は、イベント発生までの時間のパーセント点(50%点及び75%点)のKaplan-Meier推定値及びその95%CI(Brookmeyer and Crowley)を示した。
- 無月経状態の患者割合及び無月経状態となるまでの期間は、PBACスコアの合計点が10点未満である患者割合・10点未満となるまでの期間と同様の解析を行った。
- 筋腫核体積及び子宮体積のベースラインからの変化率は、対象評価時点ごとの要約統計量を示し、群間差(イセルティ®群−リュープロレリン酢酸塩群)の点推定値及びその両側95%CIを示した。また、平均値及び標準偏差を図示した。
- 血中ヘモグロビン値について、要約統計量を示し、平均値及び標準偏差を図示した。
- 血中ヘモグロビン値は、対象評価時点ごとに血中ヘモグロビン値を12g/dL未満、12g/dL以上の評価区分に分類し、例数及び割合を示した。
有効性に関するサブグループ解析
- 主要評価項目(治験薬投与6週後から12週後までのPBACスコアの合計点が10点未満である患者割合)におけるベースラインのPBACスコアの合計点が200点未満/200点以上の患者別の部分集団ごとに、改善例の例数及び割合とその両側95%CIを示した。
- ベースラインの血中ヘモグロビン値を12g/dL未満、12g/dL以上の評価区分に分類した。ベースラインの血中ヘモグロビン値が12g/dL未満の部分集団において対象評価時点ごとに血中ヘモグロビン値の要約統計量を示し、平均値及び標準偏差を図示した。また、血中ヘモグロビン値の頻度集計では対象評価時点ごとに血中ヘモグロビン値が12g/dL以上となった例数及び割合を示した。
安全性評価項目
- 群ごとの副作用の発現例数、発現割合を示した。
- 骨密度のベースラインからの変化率は、要約統計量(平均値±標準偏差)を示した。
- 治験薬最終投与から月経回復までの期間の要約統計量を示した。
患者背景
| イセルティ®群(n=143) | リュープロレリン酢酸塩群(n=144) | 全体 (n=287) |
|
|---|---|---|---|
| 年齢(歳) | |||
| 平均値±標準偏差 | 43.7±5.2 | 43.7±5.2 | 43.7±5.2 |
| 40歳未満 n(%) | 22(15.4) | 24(16.7) | 46(16.0) |
| 40歳以上 n(%) | 121(84.6) | 120(83.3) | 241(84.0) |
| 体重(kg) | |||
| 平均値±標準偏差 | 58.90±9.77 | 60.13±10.13 | 59.52±9.95 |
| BMI(kg/m2) | |||
| 平均値±標準偏差 | 23.28±3.62 | 23.63±3.78 | 23.46±3.70 |
| 子宮筋腫の種類 n(%) | |||
| 漿膜下筋腫 | 59(41.3) | 50(34.7) | 109(38.0) |
| 筋層内筋腫 | 125(87.4) | 122(84.7) | 247(86.1) |
| 粘膜下筋腫 | 24(16.8) | 33(22.9) | 57(19.9) |
| 子宮頸部筋腫 | 3(2.1) | 3(2.1) | 6(2.1) |
| 子宮筋腫既往期間(年) | |||
| 平均値±標準偏差 | 6.75±6.50 | 6.85±6.86 | 6.80±6.67 |
| 出産経験 n(%) | |||
| なし | 72(50.3) | 70(48.6) | 142(49.5) |
| あり | 71(49.7) | 74(51.4) | 145(50.5) |
| 子宮筋腫に対する薬物治療歴 n(%) | |||
| なし | 102(71.3) | 93(64.6) | 195(67.9) |
| あり | 41(28.7) | 51(35.4) | 92(32.1) |
| 子宮筋腫に対する手術歴 n(%) | |||
| なし | 122(85.3) | 124(86.1) | 246(85.7) |
| あり | 21(14.7) | 20(13.9) | 41(14.3) |
| 筋腫核体積(cm3) | |||
| 平均値±標準偏差 | 121.94±148.56 | 113.76±140.48 | 117.84±144.36 |
| 子宮体積(cm3) | |||
| 平均値±標準偏差 | 291.14±234.63 | 284.70±205.23 | 287.91±220.01 |
| 総PBACスコア*1(点) | |||
| 平均値±標準偏差 | 271.8±154.2 | 297.5±187.2 | 284.7±171.7 |
| 200未満 n(%) | 56(39.2) | 58(40.3) | 114(39.7) |
| 200以上 n(%) | 87(60.8) | 86(59.7) | 173(60.3) |
| 最大NRSスコア*2 | |||
| 平均値±標準偏差 | 3.5±2.4 | 3.8±2.4 | 3.7±2.4 |
| 血中ヘモグロビン値(g/dL) | |||
| 平均値±標準偏差 | 11.94±1.39 | 11.90±1.45 | 11.92±1.41 |
| 12未満 n(%) | 67(46.9) | 60(41.7) | 127(44.3) |
| 12以上 n(%) | 76(53.1) | 84(58.3) | 160(55.7) |
| リュープロレリン酢酸塩投与量(mg) | |||
| 1.88 n(%) | 114(79.7) | 117(81.3) | 231(80.5) |
| 3.75 n(%) | 29(20.3) | 27(18.8) | 56(19.5) |
*1:PBACスコア参照、*2:NRSスコア参照
評価スコア
*1:PBACスコア2)
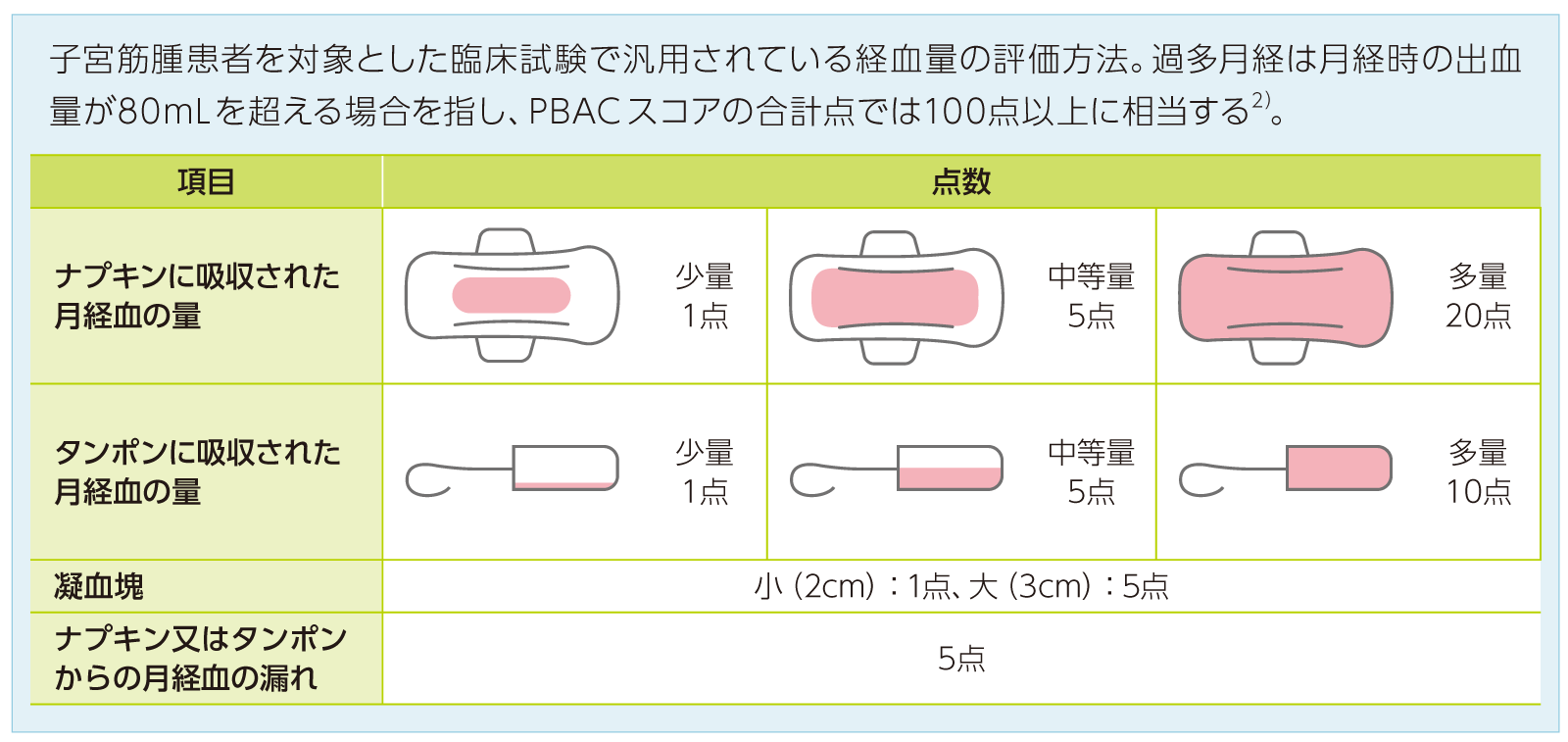
2)Higham JM, et al. Br J Obstet Gynaecol. 1990(8); 97: 734-739
算出方法
§:筋腫核体積及び子宮体積の算出方法

- 6. 用法及び用量 通常、成人にはリンザゴリクスとして200mgを1日1回経口投与する。なお、初回投与は月経周期1~5日目に行う。
- 7. 用法及び用量に関連する注意(抜粋)
- 7.1治療に際しては妊娠していないことを確認し、必ず月経周期1~5日目より投与を開始すること。
また、治療期間中は非ホルモン性の避妊をさせること。[2.1、9.5参照]





