国内第Ⅲ相臨床試験(KLH2301)1)
1)社内資料(承認時評価資料):国内第Ⅲ相臨床試験(KLH2301)(CTD2.7.6.12)
安全性
副作用
副作用の発現割合は、イセルティ®群83.9%(120/143例)及びリュープロレリン酢酸塩群91.0%(131/144例)であった。
主な副作用(いずれかの投与群で5%以上に認められた副作用)
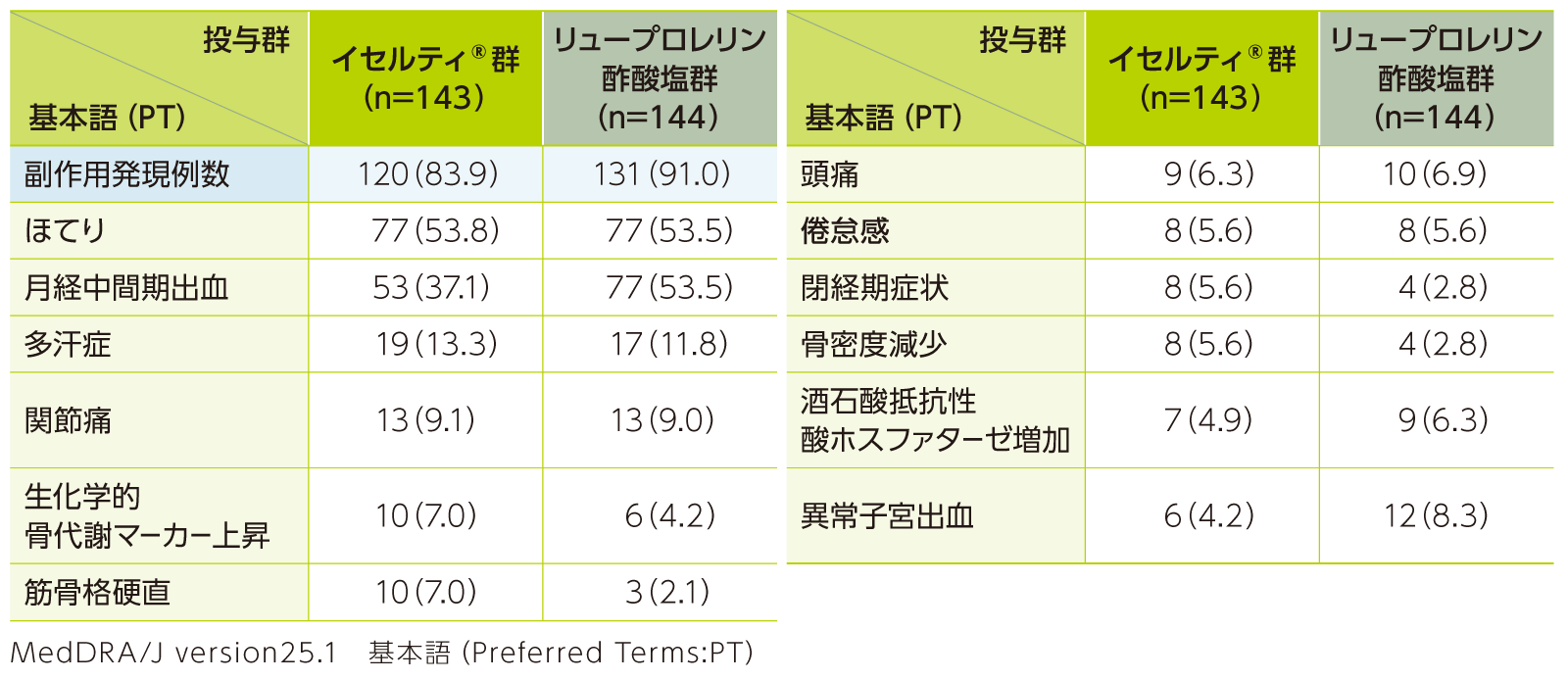
本試験において死亡に至った副作用は認められなかった。
重篤な副作用は、イセルティ®群でくも膜下出血1例、リュープロレリン酢酸塩群で異常子宮出血1例に認められた。
投与中止に至った副作用は、イセルティ®群8例5.6%(うつ病、頭痛、くも膜下出血、ほてり、肝機能異常、脱毛症、多汗症、筋骨格硬直、閉経期症状が各1例)、リュープロレリン酢酸塩群6例4.2%(閉経期症状2例、うつ病、抑うつ気分、浮動性めまい、脱毛症が各1例)であった。
骨密度のベースラインからの変化率
骨密度のベースラインからの変化率の推移は、以下のとおりであった。
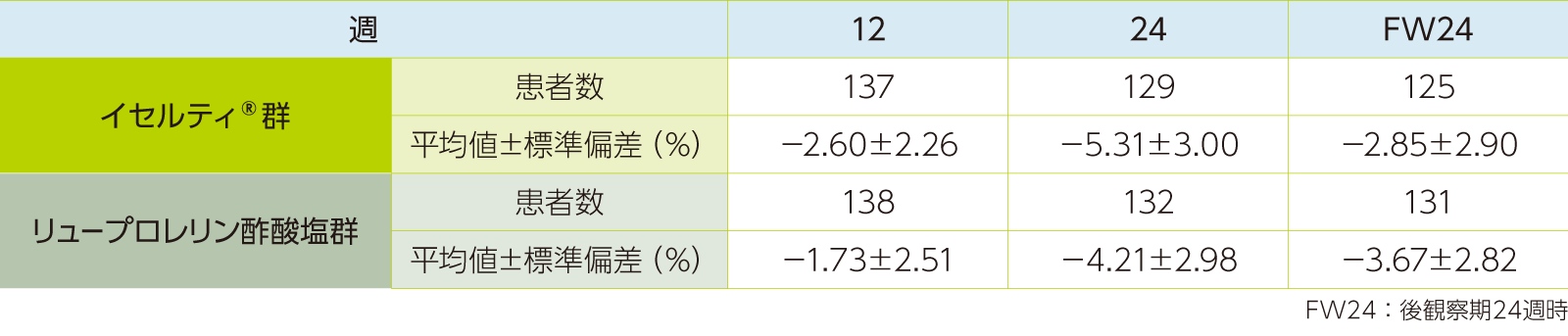
(ベースライン値)イセルティ®群:1.1359±0.1721g/cm²、リュープロレリン酢酸塩群:1.1425±0.1587g/cm²
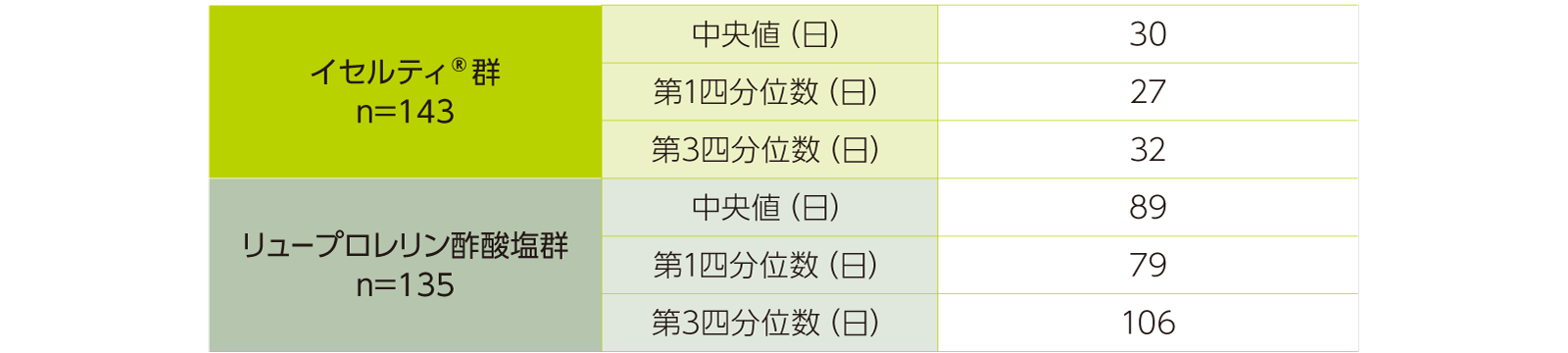
治験薬最終投与から月経回復までの期間
治験薬最終投与から月経回復までの期間の中央値は、イセルティ® 群で30日、リュープロレリン酢酸塩群で89日であった。