特性4薬物代謝酵素(CYP)による代謝を受けず(in vitro)、血液透析患者の主要な排泄経路は糞中排泄及び透析による除去でした(外国人データ)。
CYPによる代謝の影響
- シトクロムP450(CYP)に対する基質性1)
-
リコンビナントヒトCYP酵素発現系(CYP1A2、CYP2C8、CYP2C9、CYP2C19、CYP2D6及びCYP3A4)にジフェリケファリンを添加し検討した結果から、ジフェリケファリンは各CYP 分子種の基質とならないことが示唆された。
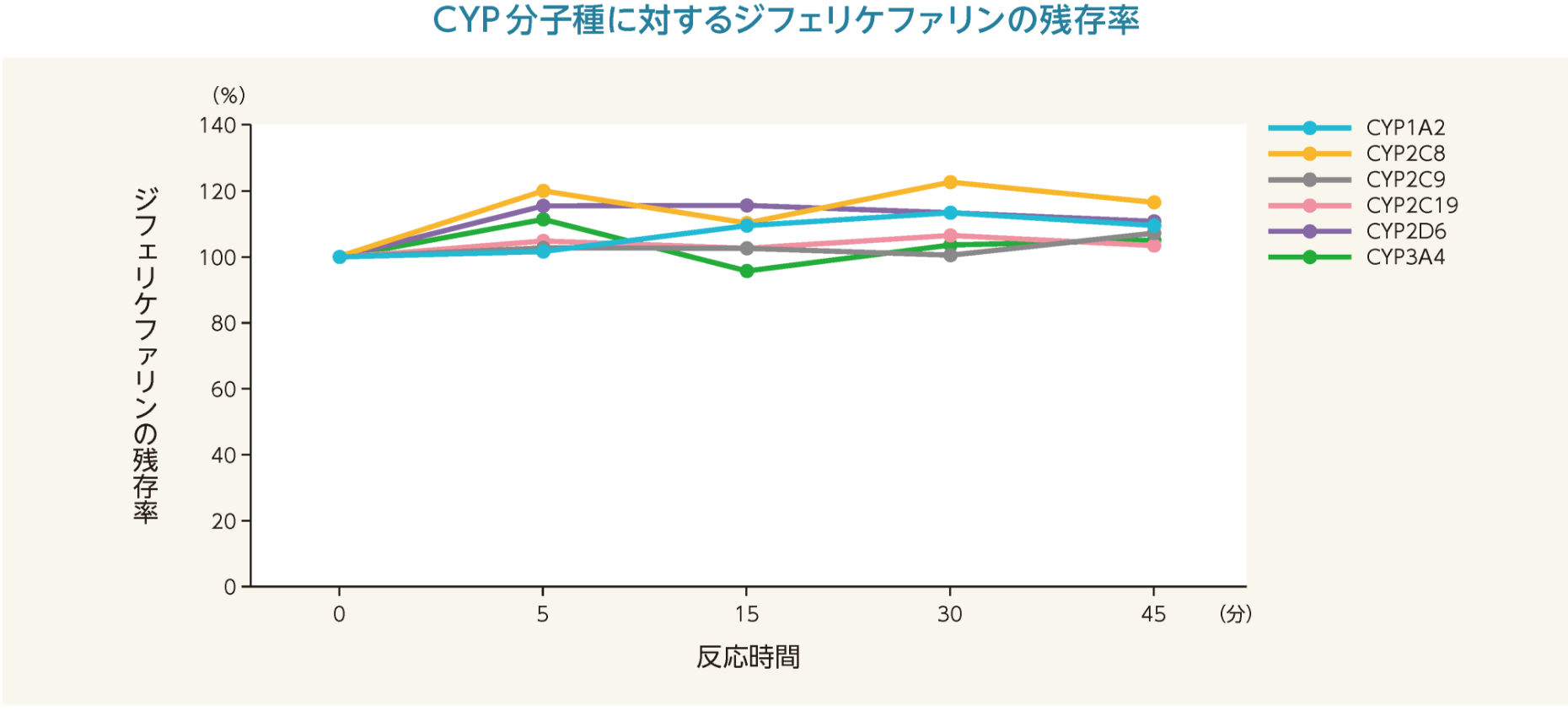
- 方法
- リコンビナントヒトCYP酵素発現系(BactosomesTM)を用いて主要な6種のヒトCYP分子種(CYP1A2、CYP2C8、CYP2C9、CYP2C19、CYP2D6、CYP3A4)について、ジフェリケファリンを45分間反応させたときのジフェリケファリンの残存率から評価した。
1)社内資料:in vitro代謝試験(2023年9月25日承認、CTD2.6.4.5.1)
主要な排泄経路
- 健康成人及び血液透析患者(外国人データ)1)
-
健康成人におけるジフェリケファリンの主な消失経路は尿中であり、投与放射能量の約80%が排泄された。
血液透析患者6例に14C-ジフェリケファリン230 μg(1.7 ~ 3.0 μg/kg)注)を単回静脈内投与したとき、投与した放射能の58.8%が糞中、19.5%が透析液中及び11.2%が尿中に排泄された。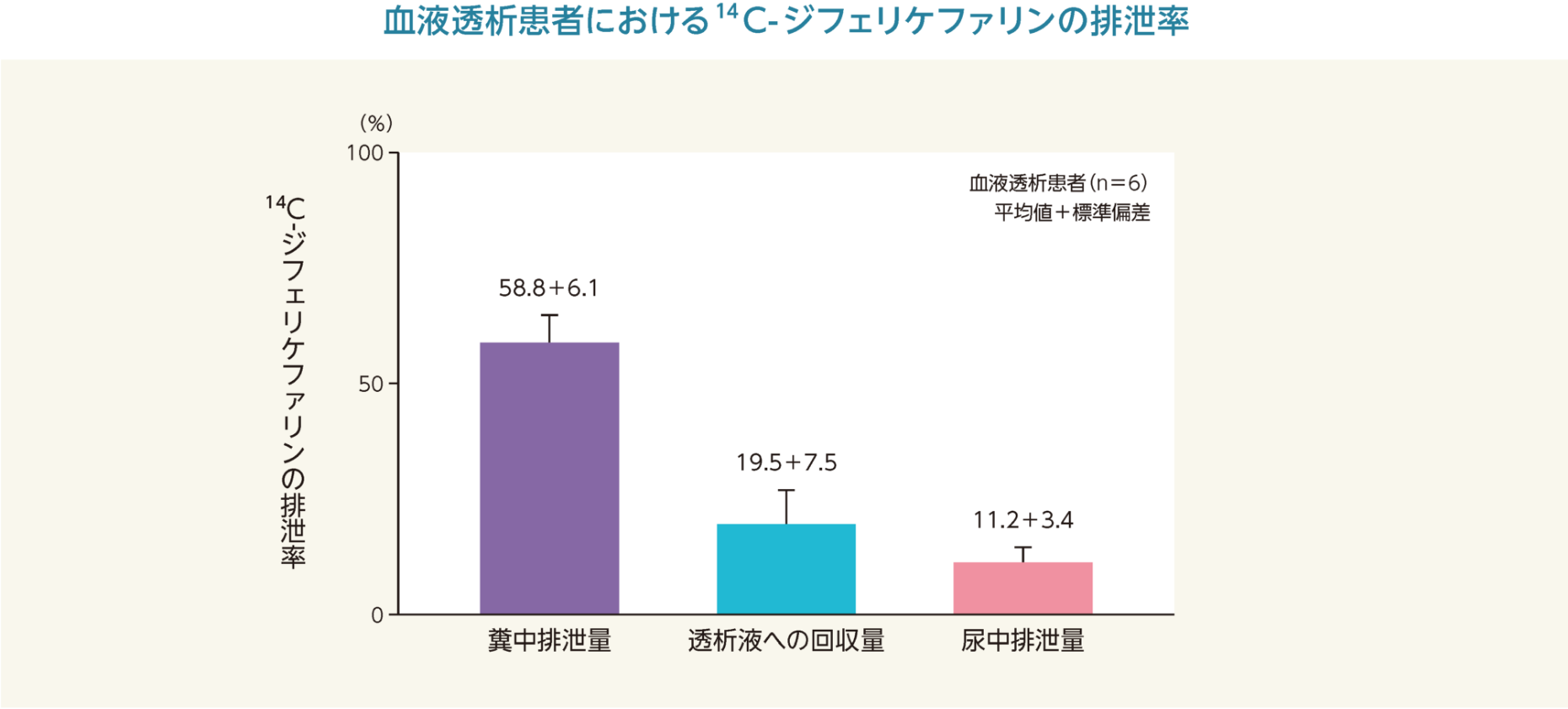
- 対象
- 18歳以上の男性非喫煙者である、血液透析患者6例と健康成人6例を対象とした、第I相、単施設、非盲検、単回放射性標識体投与、非無作為化試験として実施した。
- 方法
- すべての被験者はDay 1に14C-ジフェリケファリンを単回静脈内ボーラス投与された。14C-ジフェリケファリンの薬物動態及びマスバランスを評価するために、規定された時間に血液、尿及び糞便のサンプルを採取した。
注)承認用量は0.5 μg/kgをベースとしたドライウェイトに基づく体重区分ごとの投与量
45.0 kg未満:17.5 μg、45.0 kg以上65.0 kg未満:25.0 μg、65.0 kg以上85.0 kg未満:35.0 μg、85.0 kg以上:42.5 μgである。1)社内資料:海外マスバランス試験(CR845-100302)(2023年9月25日承認、CTD2.7.2.2.2.3.4)





