薬効薬理
1.作用機序
(1)DPP-4阻害作用6)
オマリグリプチンは、インクレチン(GLP-1及びGIP)を分解する酵素であるDPP-4を阻害することによって、活性型インクレチン濃度を上昇させ、血糖依存的にインスリン分泌促進作用及びグルカゴン分泌抑制作用を増強して血糖管理を改善します。
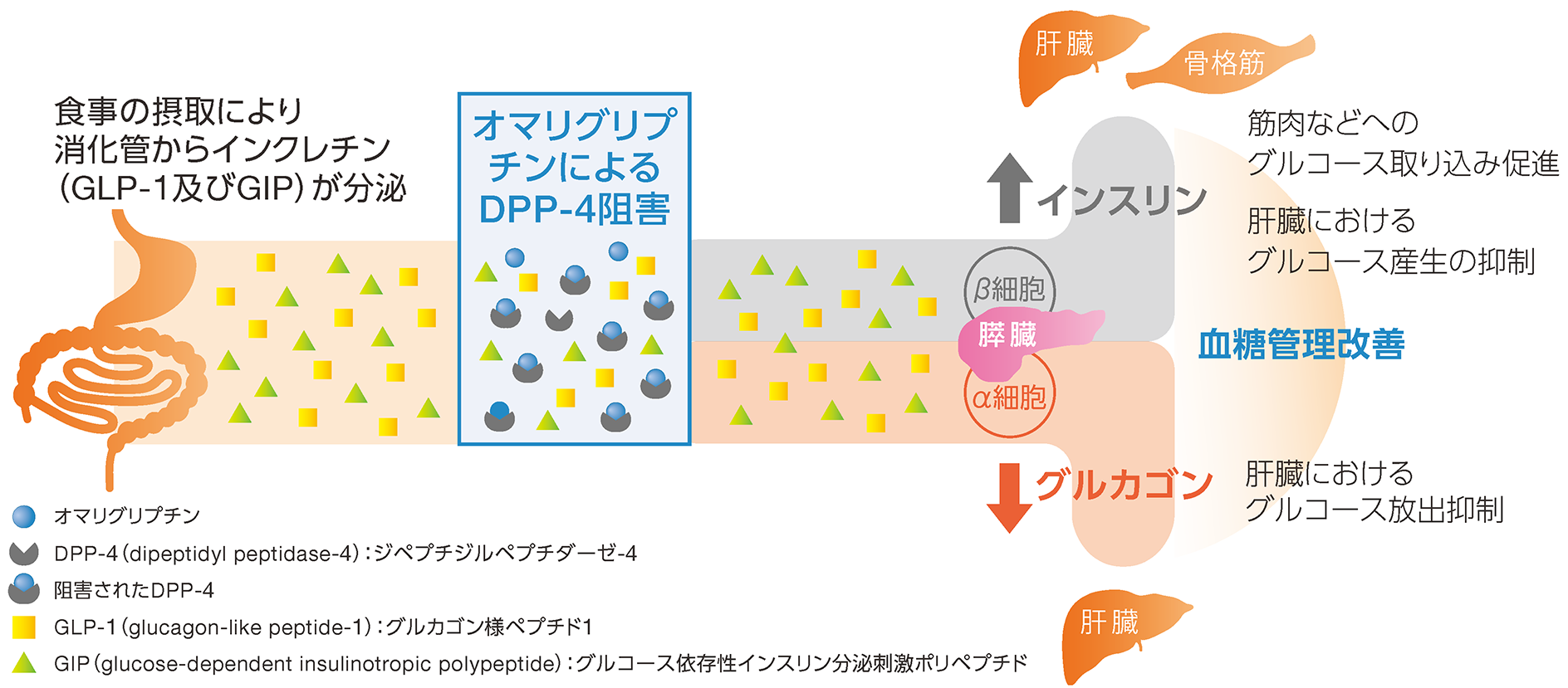
6)Plosker GL. Drugs. 2014; 74: 223-242.より作図
(2)長時間作用するメカニズム7、8、9、10)
オマリグリプチンの肝臓による代謝は糞中の総放射能排泄率3.36%であり、未変化体として体内に分布しました(ヒト)。そのため投与1時間後には血漿や副腎、横隔膜など、全身の組織でオマリグリプチン由来の放射能が最高濃度に到達しました(動物種:ラット)。腎糸球体で濾過されたのち、大部分が尿細管で受動的に再吸収され、体内循環を繰り返します。
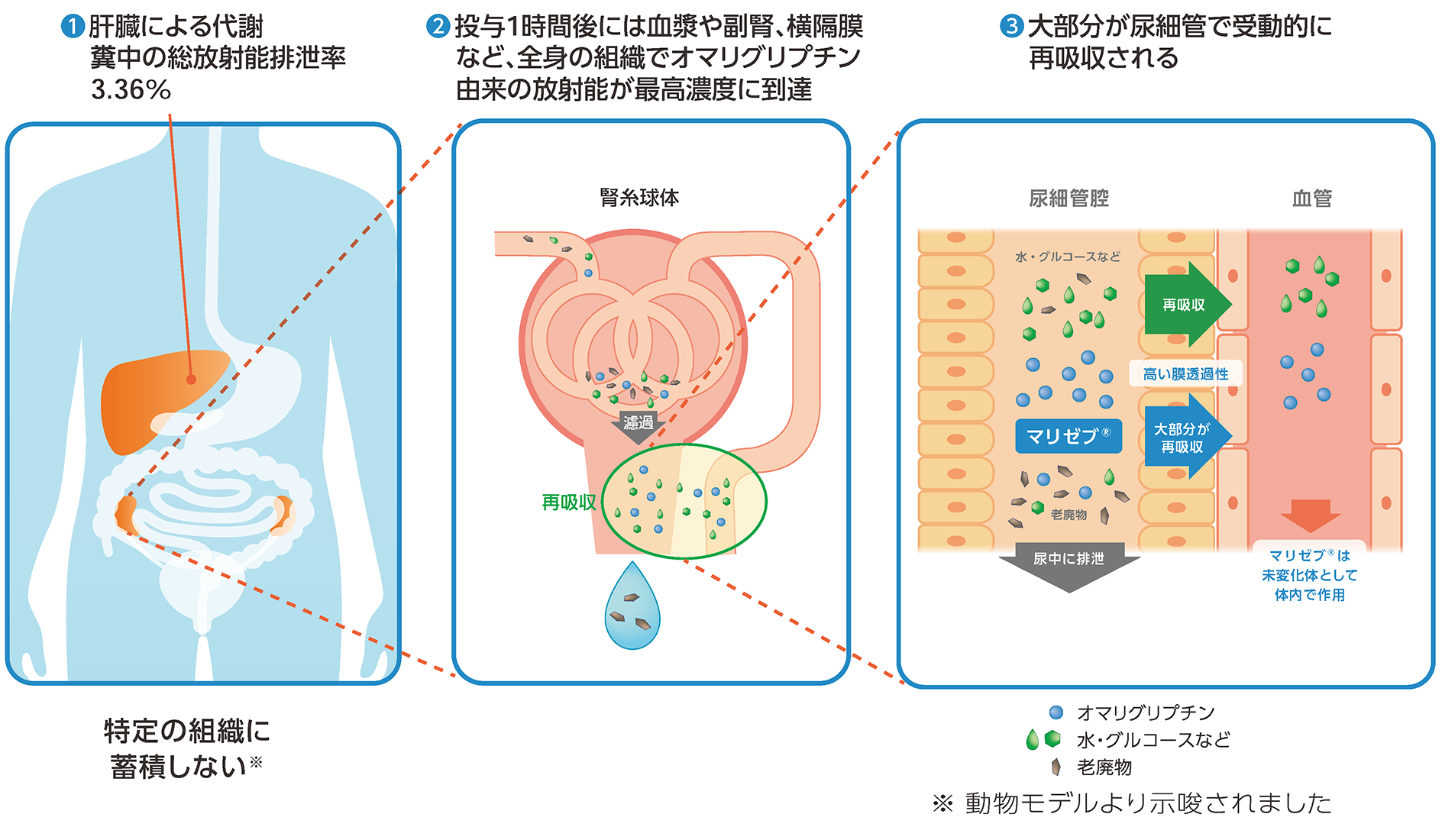
7)社内資料(承認時評価資料):日本人健康被験者を対象とした単回及び反復投与試験(P005)(2015年9月28日承認、CTD2.7.6.2.3)
8)社内資料(承認時評価資料):非日本人健康被験者を対象としたマスバランス試験(P007)(2015年9月28日承認、CTD2.7.6.2.6)
9)社内資料(承認時評価資料):ラットにおける組織分布(2015年9月28日承認、CTD2.6.4.4.1)
10)社内資料(承認時評価資料):非日本人健康被験者を対象とした反復投与試験(P002)(2015年9月28日承認、CTD2.7.6.2.5)
2.臨床薬理試験
(1)DPP-4阻害作用(海外データ)7)
健康成人6例に、オマリグリプチン25mgを週1回3週間反復経口投与した結果、オマリグリプチン投与3回目の投与7日後のDPP-4阻害率(最小二乗平均値、ベースラインで補正)は88%でした。
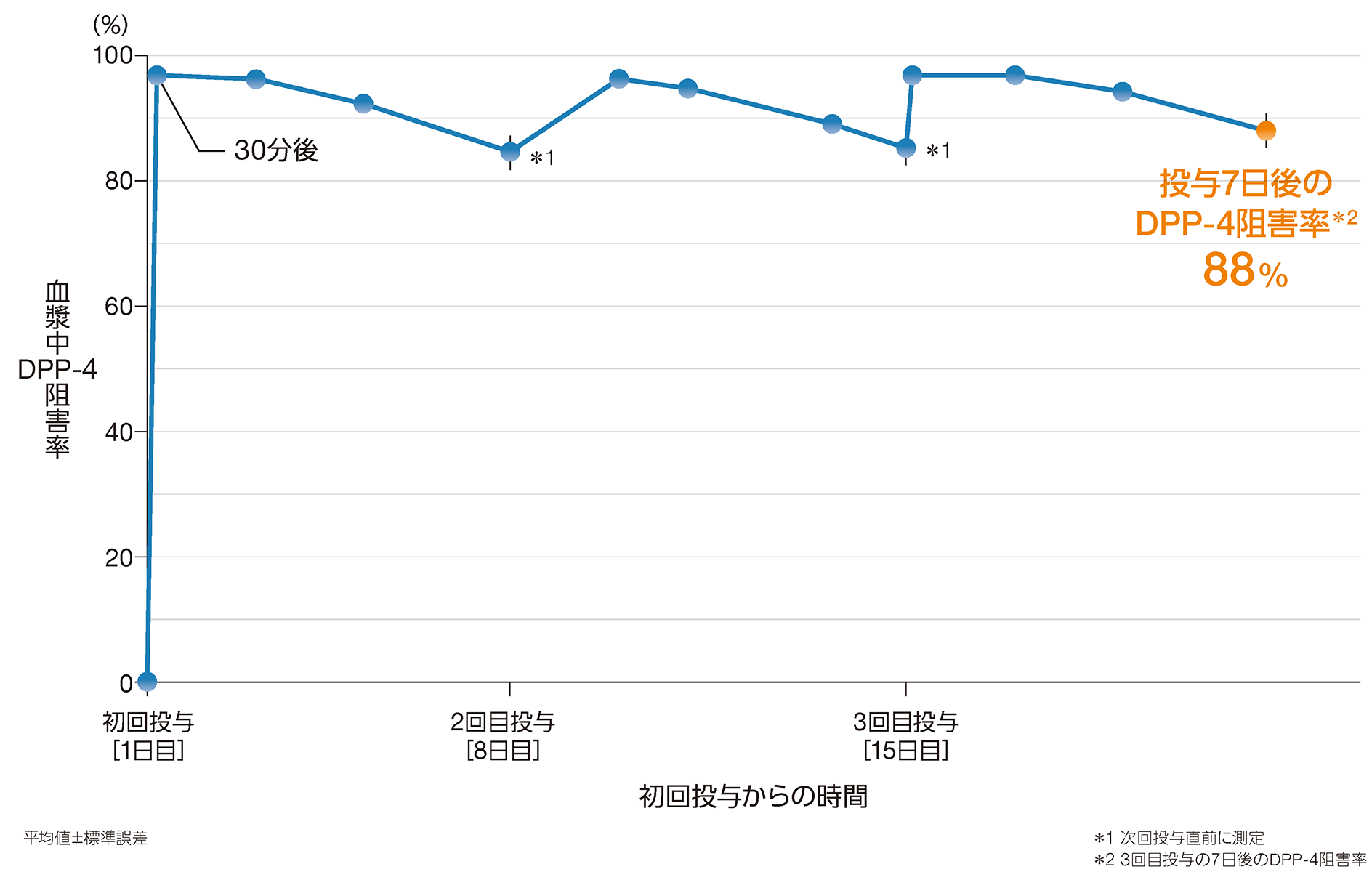
7)社内資料(承認時評価資料):日本人健康被験者を対象とした単回及び反復投与試験(P005)(2015年9月28日承認、CTD2.7.6.2.3)
- 対象
- 海外在住日本人健康成人男性6例
- 方法
- オマリグリプチン1~50mgを週1回3週間反復経口投与した。
- 解析計画
- 高血漿中濃度による分析(蛍光法)及び低血漿中濃度による分析(吸光光度法)によりDPP-4阻害率を測定。ベースラインを第1日の治験薬投与前の値とし、処置と投与日の交互作用を固定効果、被験者を変量効果とする線形混合効果モデルを用いて解析した。
(2)活性型GLP-1濃度に及ぼす影響(海外データ)10)
健康成人6例に、オマリグリプチン25mgを週1回3週間反復経口投与しました。3回目投与(15日目)の投与10時間後に食事を摂取し、食後2時間における血漿中活性型GLP-1濃度を測定した結果、ベースライン時からの加重平均値の増加〔幾何平均値[95%信頼区間]〕は、オマリグリプチン25mg/週 群では3.07[2.40、3.92]、プラセボ群では1.50[1.21、1.85]でした。プラセボ群との幾何平均比[90%信頼区間]は2.05[1.57、2.67]であり、90%信頼区間の下限は1を上回りました。
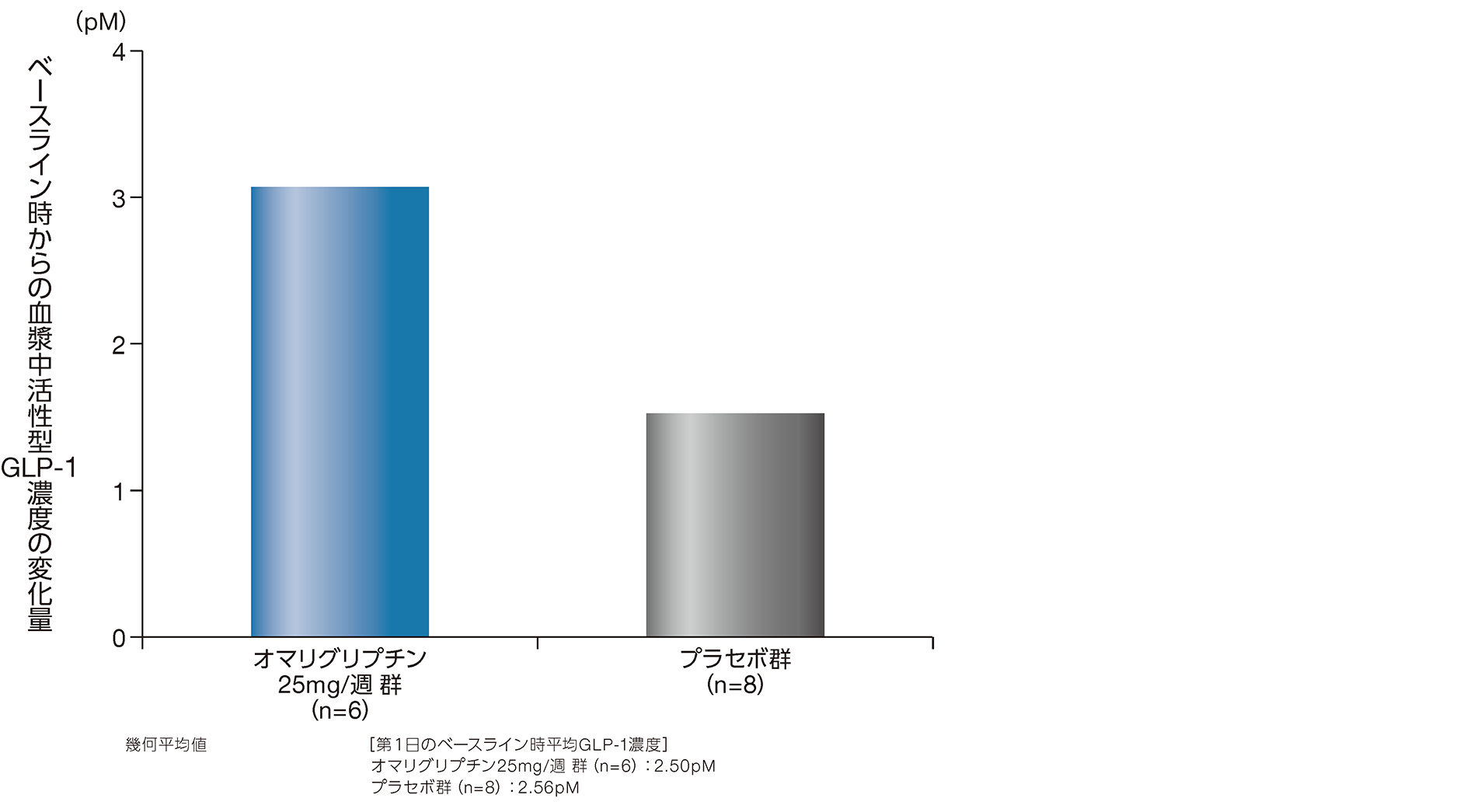
10)社内資料(承認時評価資料):非日本人健康被験者を対象とした反復投与試験(P002)(2015年9月28日承認、CTD2.7.6.2.5)
- 対象
- 健康成人男性(19~44歳)6~8例
- 方法
- オマリグリプチン25mg/週を3週間反復経口投与した。
- 解析計画
- オマリグリプチン投与後の血漿中のGLP-1濃度の変動を検証した。
テストミール負荷後2時間における加重幾何平均値
(3)QT/QTcに及ぼす影響(海外データ)11)
健康成人53例を対象に、1日目にオマリグリプチン25mg、2日目にオマリグリプチン175mgを単回投与した結果、ベースラインからのQTcP変化量のプラセボとの平均値の差は、すべての投与後測定時点で10msec未満となりました。最小二乗平均値の差の最大値は3.66msec、その90%信頼区間は[1.56、5.76]でした。
QTcP(Population-specific heart rate correction for QT): 母集団データに基づき補正したQT間隔
11)社内資料(承認時評価資料):非日本人健康被験者を対象とした QT/QTc 評価試験(P010)(2015年9月28日承認、CTD2.7.6.2.16)
3.非臨床試験
(1)DPP-4阻害作用(in vitro)12)
オマリグリプチンのヒト組換え型DPP-4に対するIC50値は1.6nMで、解離定数(Ki)は0.8nMでした。さらに、ヒト血清由来DPP-4に対するIC50値は低濃度(2%)血清存在下では2.1nM、高濃度(50%)血清存在下では6.7nMでした。
一方、標的外分子であるDPP-8、DPP-9、QPP、PEP及びFAPに対するオマリグリプチンのIC50値は>100,000nMでした。
| n(例数) | IC 50(nM) | |
|---|---|---|
| ヒト組換え型DPP-4 | 3 | 1.6±0.03 |
| ヒト血清DPP-4(2%血清存在下) | 3 | 2.1±0.08 |
| ヒト血清DPP-4(50%血清存在下) | 3 | 6.7±0.13 |
平均値±標準偏差
| n(例数) | IC 50(nM) | |
|---|---|---|
| DPP-8 | 2 | >100,000 |
| DPP-9 | 1 | >100,000 |
| QPP | 2 | >100,000 |
| PEP | 2 | >100,000 |
| FAP | 2 | >100,000 |
平均値
12) 社内資料(承認時評価資料):オマリグリプチンのin vitro 及びin vivo 薬理試験(2015年9月28日承認、CTD2.6.2.2)
DPP-8(dipeptidyl peptidase-8):ジペプチジルペプチダーゼ-8
DPP-9(dipeptidyl peptidase-9):ジペプチジルペプチダーゼ-9
QPP:quiescent cell proline dipeptidase
PEP:prolyl endopeptidase
FAP:fibroblast activation protein
- 方法
- DPP-4及び標的外分子(DPP-8、DPP-9、QPP、PEP、FAP)に対するオマリグリプチンの阻害活性について連続蛍光分析法を用いて検討した。
(2)耐糖能及び糖代謝改善作用(マウス)
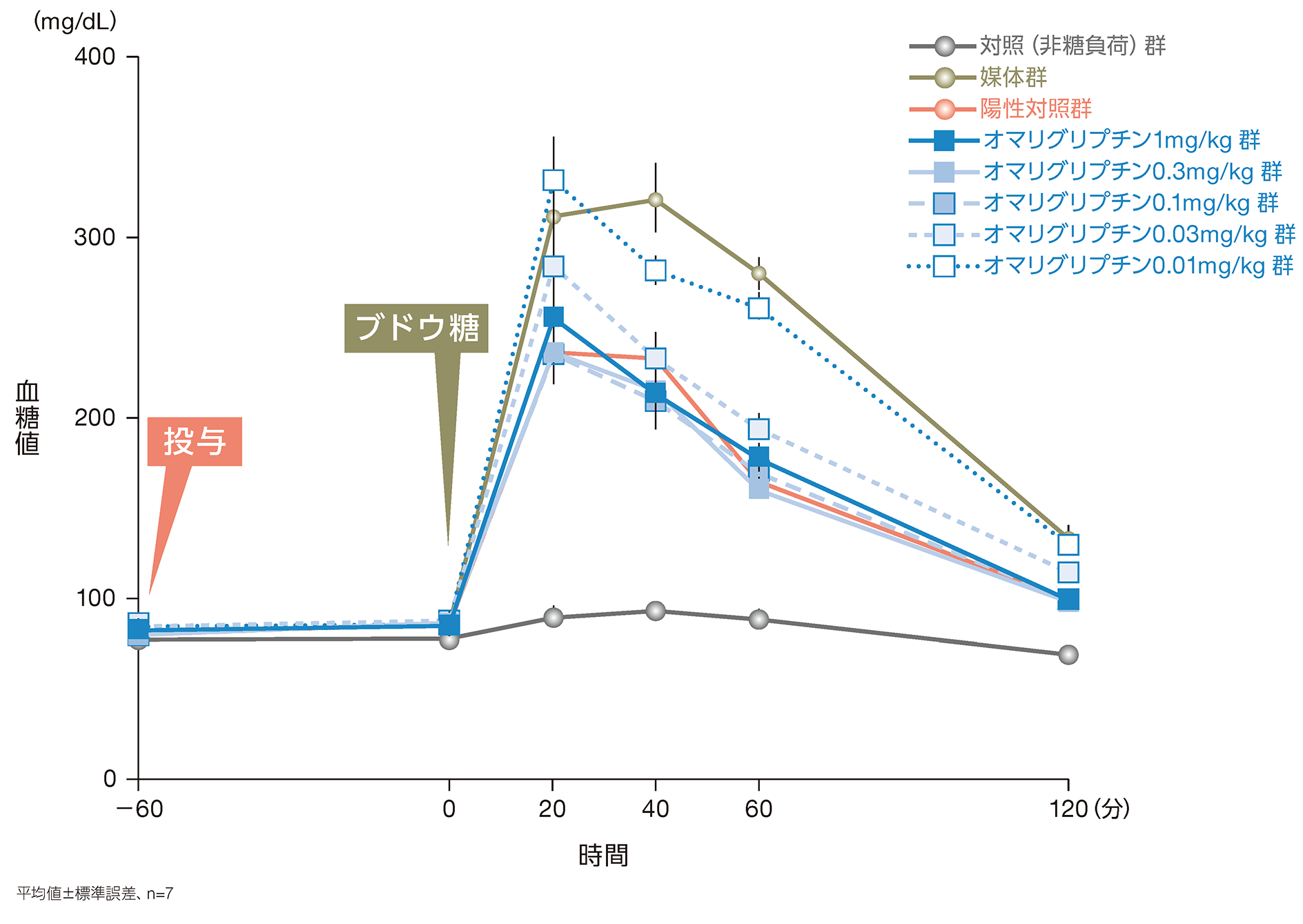
①正常マウスの耐糖能に対するオマリグリプチン単回経口投与の影響12)
正常マウスを用いた経口ブドウ糖負荷試験(OGTT)において、オマリグリプチンはブドウ糖負荷後の血糖値の上昇を抑制しました。
12) 社内資料(承認時評価資料):オマリグリプチンのin vitro 及びin vivo 薬理試験(2015年9月28日承認、CTD2.6.2.2)
- 対象
- 一晩絶食させた雄性C57BL/6N マウス(7例/群)
- 方法
- 媒体(0.25%メチルセルロース水溶液)、オマリグリプチン0.01、0.03、0.1、0.3、1mg/kgまたは陽性対照(デスフルオロシタグリプチン3mg/kg)を経口投与し、その60分後にブドウ糖5g/kgを経口負荷した。非糖負荷対照として、媒体を投与し水を経口負荷した群を設けた。
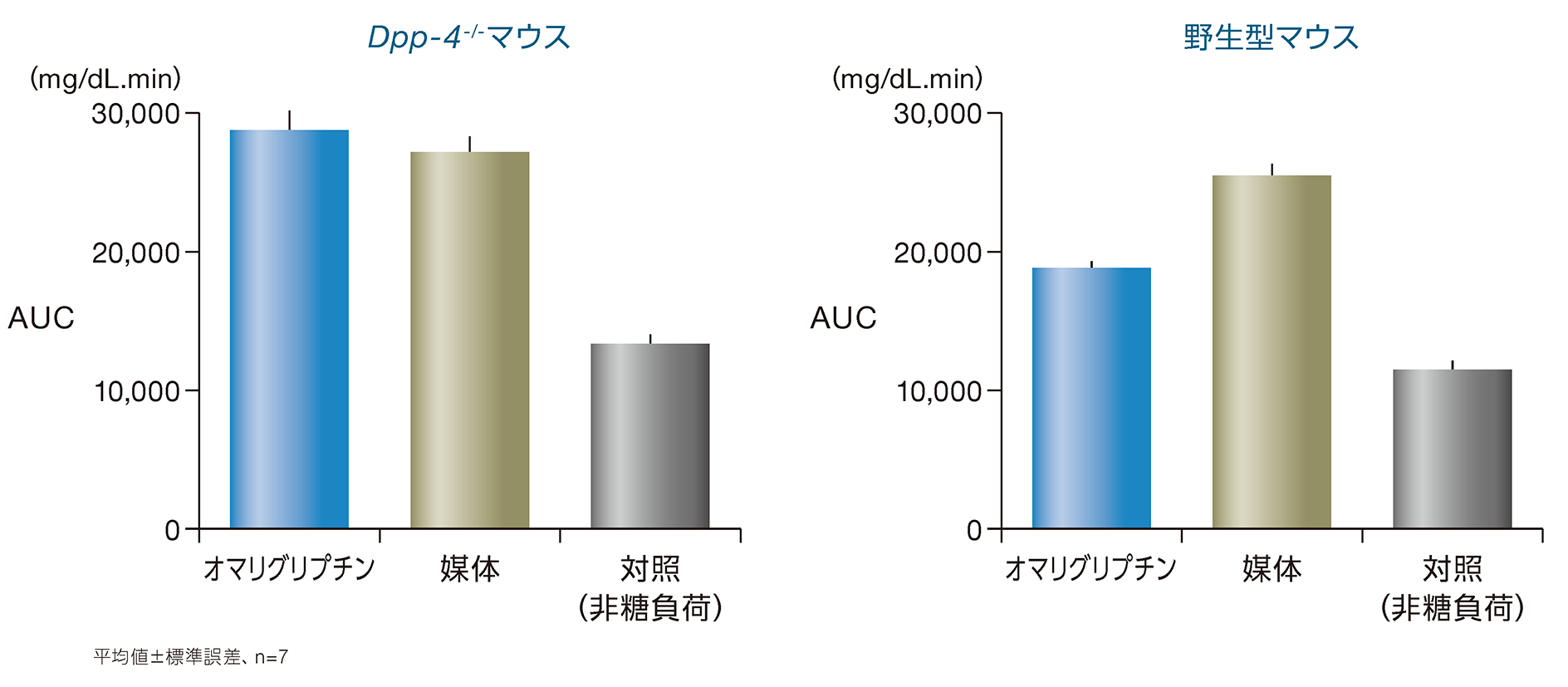
②Dpp-4-/-マウス及び野生型マウスにおけるオマリグリプチン単回経口投与の血糖降下作用12)
DPP-4欠損(Dpp-4-/-)マウス及び野生型マウスを用いたOGTTにおいて、オマリグリプチンを単回経口投与した結果、野生型マウスの血糖値上昇を抑制しましたが、Dpp-4-/-マウスの血糖値上昇は抑制しませんでした。
12) 社内資料(承認時評価資料):オマリグリプチンのin vitro 及びin vivo 薬理試験(2015年9月28日承認、CTD2.6.2.2)
- 対象
- 一晩絶食させた雄性Dpp-4-/-マウスまたは野生型マウス(7例/群)
- 方法
- 媒体(0.25%メチルセルロース水溶液)またはオマリグリプチン3mg/kgを経口投与し、その60分後にブドウ糖5g/kgを経口負荷した。非糖負荷対照として、媒体を投与し水を経口負荷した群を設けた。
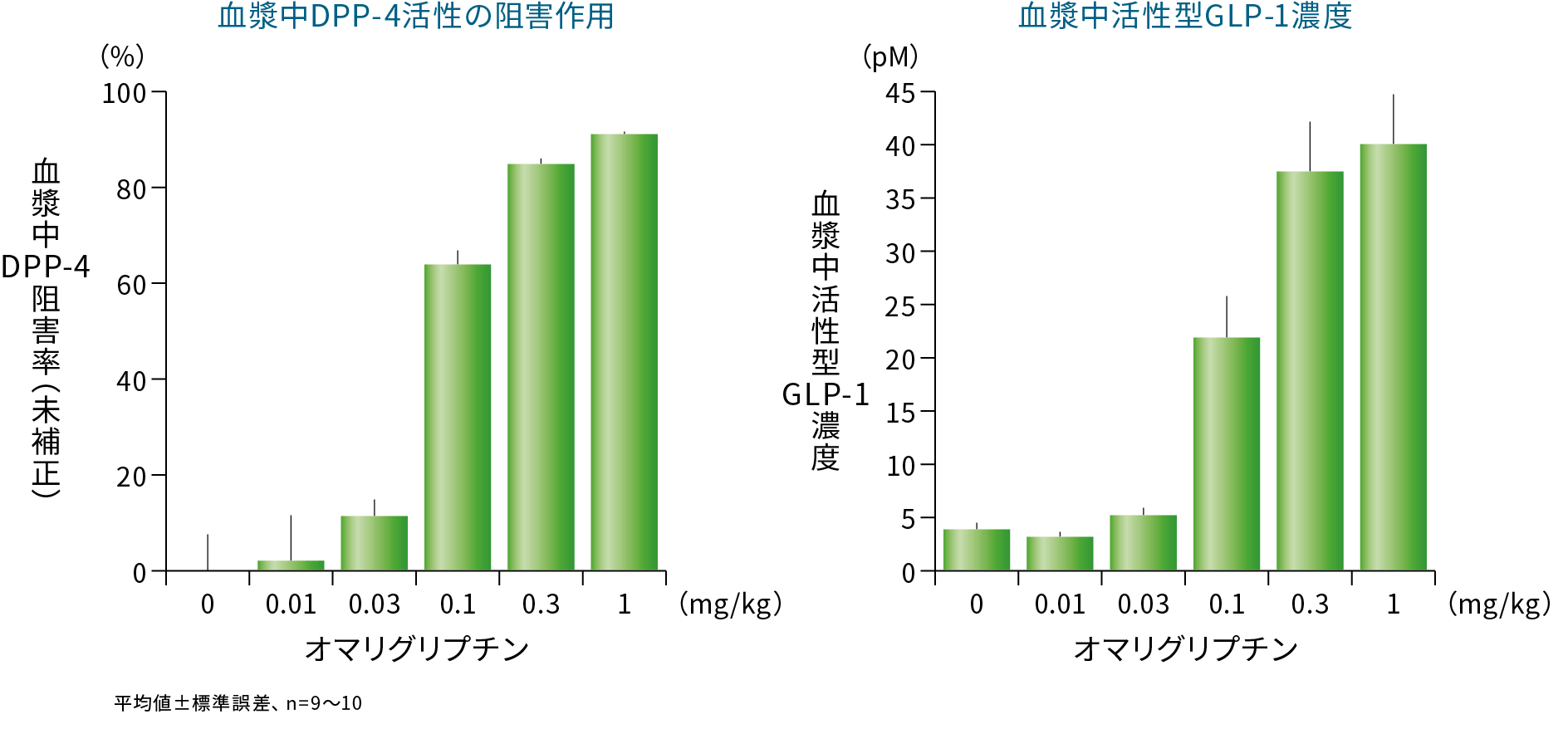
③正常マウスにおけるオマリグリプチン単回経口投与の血漿中DPP-4活性及び活性型GLP-1濃度への影響12)
正常マウスを用いたOGTTにおいて、オマリグリプチンは血漿中DPP-4活性を阻害し、血漿中活性型GLP-1濃度が上昇しました。
12) 社内資料(承認時評価資料):オマリグリプチンのin vitro 及びin vivo 薬理試験(2015年9月28日承認、CTD2.6.2.2)
- 対象
- 一晩絶食させた雄性C57BL/6N マウス(9~10例/群)
- 方法
- 媒体(0.25%メチルセルロース水溶液)またはオマリグリプチン0.01、0.03、0.1、0.3、1mg/kgを経口投与し、その60分後にブドウ糖5g/kgを経口負荷した。ブドウ糖負荷10分後に採血し、血漿中のDPP-4活性及び活性型GLP-1濃度を測定した。





