■海外第Ⅱ/Ⅲ相臨床試験(海外データ)8)、9)
8)承認時評価資料:海外第Ⅱ/Ⅲ相臨床試験(TT02)
9)添付文書改訂時評価資料:海外第Ⅱ/Ⅲ相臨床試験(TT02)
目的
アントラサイクリン系抗悪性腫瘍剤の血管外漏出に対するデクスラゾキサンの有効性と安全性を検討した
試験デザイン
多施設共同非盲検試験
対象
アントラサイクリン系抗悪性腫瘍剤の血管外漏出患者57例
(有効性評価例数:蛍光法による組織生検で血管外漏出が確認された36例、安全性評価例数:57例)
方法
投与1日目(発生から6時間以内)及び2日目(初回投与開始24時間後)はデクスラゾキサン1000mg/m2を、3日目(初回投与開始48時間後)は500mg/m2を1日1回、1~2時間かけて3日間連日静脈内投与した。
評価項目
1)有効性(評価期間:90日)
主要評価項目
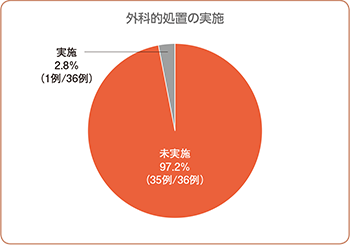
・血管外漏出に対する外科的処置率
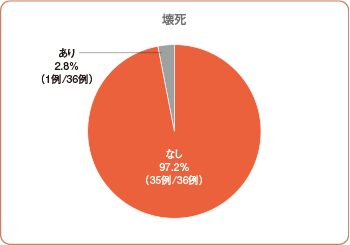
・壊死
副次評価項目
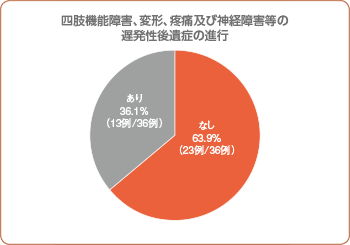
・四肢機能障害、変形、疼痛及び神経障害等の遅発性後遺症の進行
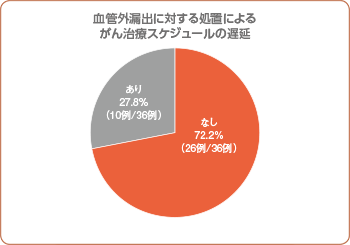
・血管外漏出に対する処置によるがん治療スケジュールの遅延
2)安全性(評価期間:28日)
・デクスラゾキサン投与開始後4週間の毒性評価(NCI-CTC)
・有害事象
・臨床検査
解析計画
血管外漏出に対する外科的処置率については、文献調査よりアントラサイクリン系抗悪性腫瘍剤の血管外漏出患者の約35〜50%で進行性の症状・所見のために外科的処置が必要と考えられたことから、外科的処置の発生率が35%を下回る場合に有効と評価した。p値は35%の帰無仮説に対しての正確な2項検定により算出した。
安全性は、有害事象(重篤な有害事象を含む)の発現状況及び臨床検査により評価した。有害事象の重症度は、NCI-CTC規準(第2.0版)に基づくグレード判定と因果関係を評価した。
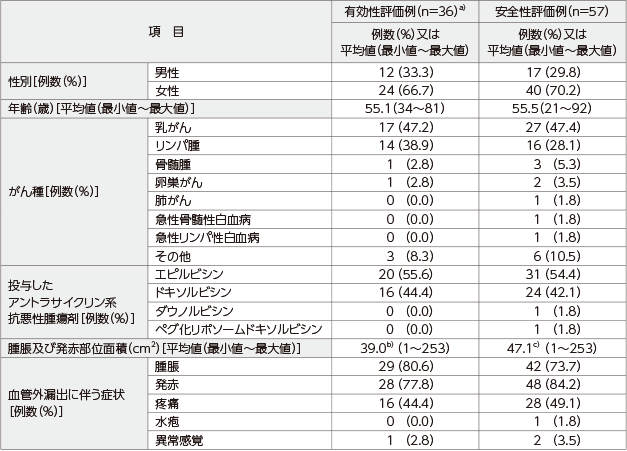
a)除外された21例の内訳:
「生検陰性」9例
「実施計画書からの逸脱」12例
b)面積不明の1例を除く35例の平均値
c)面積不明の3例を除く54例の平均値
本剤投与後、外科的処置を実施した症例は36例中1例(2.8%)であり、デクスラゾキサンの有効性が認められました(両側95%信頼区間:0.1~14.5%、p<0.0001 vs 35%、正確二項検定)。
本剤投与後、 外科的処置を実施した1例に壊死が認められました。
最終評価時において、36例中23例(63.9%)で四肢機能障害、変形、疼痛及び神経障害等の遅発性後遺症の進行を認めませんでした。その他の13例に認められた症状は、疼痛9件、感覚障害7件、皮膚萎縮4件、運動障害3件及び外観損傷1件でした。
本剤投与後、36例中26例(72.2%)で計画された化学療法を遅延なく継続しました。遅延の認められた10例のうち、1例は外科的処置を実施した症例であり、同症例を除いた9例におけるがん治療スケジュールの遅延は平均10日(最小7日、最大15日)でした。
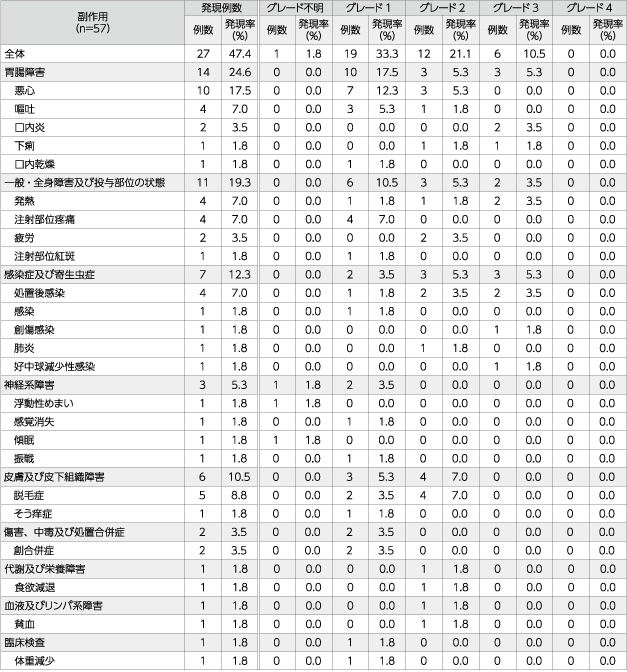
副作用の発現率は47.4%(27/57例)であり、主な副作用は悪心17.5%(10/57例)、脱毛症8.8%(5/57例)、注射部位疼痛7.0%(4/57例)、発熱7.0%(4/57例)、嘔吐7.0%(4/57例)、処置後感染7.0%(4/57例)などでした。
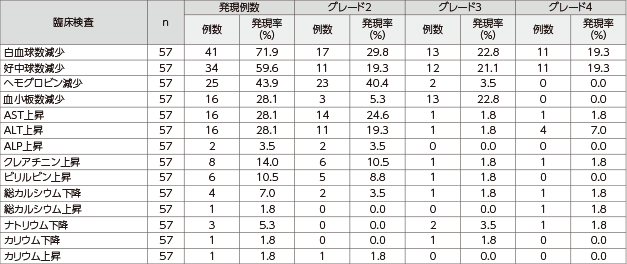
主な臨床検査値異常は白血球数減少71.9%(41/57例)、好中球数減少59.6%(34/57例)、ヘモグロビン減少43.9%(25/57例)、血小板数減少28.1%(16/57例)、AST上昇28.1%(16/57例)、ALT上昇28.1%(16/57例)、クレアチニン上昇14.0%(8/57例)及びビリルビン上昇10.5%(6/57例)などでした。
また、重篤な有害事象は発熱12.3%(7/57例)、浮動性めまい、処置後感染、肺炎、各5.3%(3/57例)、下痢3.5%(2/57例)、好中球減少性感染、腹水、食欲減退、不整脈、低カリウム症、傾眠、全身性真菌症、昏睡、腎不全、口内炎、疲労、悪心、呼吸困難、創傷感染、高血糖、発熱性好中球減少症、疾患進行、深部静脈血栓症、各1.8%(1/57例)でした。死亡は3例(気管支アスペルギルス症、発熱性好中球減少症/敗血性ショック、肺炎、各1例)報告され、いずれも治療薬との因果関係は否定されました。
重症度はNCI-CTC規準(第2版)に基づき判定した。
同一症例においてグレードの異なる同一の副作用が認められた場合、それぞれのグレードで例数をカウントした。
8. 重要な基本的注意(一部抜粋)
8.2 投与後は血管外漏出の症状が軽快するまで、定期的に漏出部位の状態を観察すること。
8.3 本剤は投与中及び投与終了後に骨髄抑制をおこすことがあるため、定期的に血液検査を行うなど、患者の状態を十分観察し、異常が認められた場合には適切な処置を行うこと。[11.1.1参照]