グルファスト錠 Q&A
「Q&A」は、医療関係者の皆様に向けて作成しています。
本内容は、製品の適正使用に関する参考情報であり、すべてのケースに当てはまるものではありません。また、国内で承認された効能効果・用法用量の範囲外の情報を含む場合がありますが、当社として推奨するものではありません。製品のご使用にあたっては、最新の電子添文をご確認ください。
「Q&A」のご利用によって、生じた結果につきましては、責任を負いかねますのでご了承ください。
※許可なく複写、複製、転掲、改変等を行うことはご遠慮ください。
-
Q1.グルファスト錠の食直前の服薬指導について教えてください。
食事の直前5分以内に服用するようご指導ください。
グルファスト錠は、食後投与では速やかな吸収が得られず効果が減弱します。効果的に食後の血糖上昇を抑制するため、グルファスト錠の投与は、毎食直前(5分以内)としてください。
また、グルファスト錠は、投与後速やかに薬効を発現するため、食前30分投与では、食前15分に血中インスリン値が上昇し、食事開始時の血糖値が低下することが報告されており、食事開始前に低血糖を誘発する可能性があります。このことからも、グルファスト錠の投与は、毎食直前(5分以内)としてください。参考資料:
電子添文
〔2025年8月改訂〕-
Q2.グルファスト錠の用法は食直前投与ですが、食後に服用するとどうなりますか?
グルファスト錠を、食後に投与して安全性、有効性を検討した報告はありません。
グルファスト錠の承認時の第Ⅰ相臨床試験(単回投与)において、健康成人男性にミチグリニドカルシウム水和物5mg(錠)を食後に経口投与注)すると、食直前に比べて、最高血漿中濃度(Cmax)の低下と最高血漿中濃度到達時間(Tmax)の遅延により効果が減弱します。この薬物動態パラメータの変化は、低血糖症状の発現に繋がるおそれがあります。
健康成人男性における食直前及び食後投与時の薬物動態パラメータ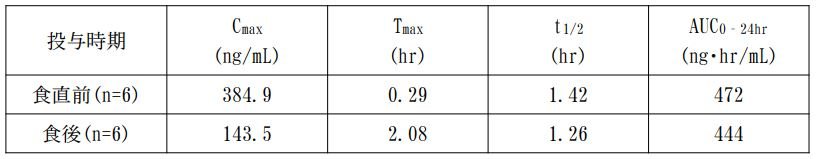
注)グルファスト錠の承認されている用法及び用量は、「通常、成人にはミチグリニドカルシウム水和物として1回10mgを1日3回毎食直前に経口投与する。なお、患者の状態に応じて適宜増減する。」です。
参考資料:
電子添文
〔2025年8月改訂〕-
Q3.グルファスト錠を食事中あるいは食後に飲み忘れに気づいた場合、どうすればよいですか?
食事中あるいは食後にグルファスト錠の飲み忘れに気づいた場合には、その回の服用はさけ、次の食事の際、食直前(5分以内)に1回分を服用してください。2回分を一度に服用したり、空腹時に服用したりしないでください。
参考資料:
グルファストを服用される患者さんへ
〔2025年8月改訂〕-
Q4.グルファスト錠はスルホニル尿素系製剤(SU剤)と併用してもよいですか?
グルファスト錠は、スルホニル尿素系製剤と、併用しないでください。
グルファスト錠は、速やかなインスリン分泌促進作用を有しています。その作用点は、スルホニル尿素系製剤と同じであり、スルホニル尿素系製剤との相加・相乗の臨床効果及び安全性は、確認されていません。参考資料:
電子添文
〔2025年8月改訂〕-
Q5.グルファスト錠の腎機能障害患者への投与に関する注意事項を教えてください。
腎機能障害患者への投与は、低血糖を起こすおそれがあるため、注意が必要です。
グルファスト錠の腎機能障害者における臨床試験において、慢性腎不全患者の血漿中薬物未変化体濃度の消失半減期が延長することが報告されています。成人腎機能正常者、腎機能低下患者及び慢性腎不全患者(ミチグリニドカルシウム水和物投与前日の平均クレアチニンクリアランス値はそれぞれ113.75、37.01及び3.431mL/min)に、ミチグリニドカルシウム水和物10mg(錠)を食直前に単回経口投与したとき注)、クレアチニンクリアランスの低下に伴い半減期(t1/2)は延長しましたが、その他の主要パラメータ(Cmax、AUC0-inf及びCLtot/F)と、クレアチニンクリアランスとの間に、有意な相関は認められませんでした。
腎機能正常者、腎機能低下者及び慢性腎不全患者における薬物動態パラメータ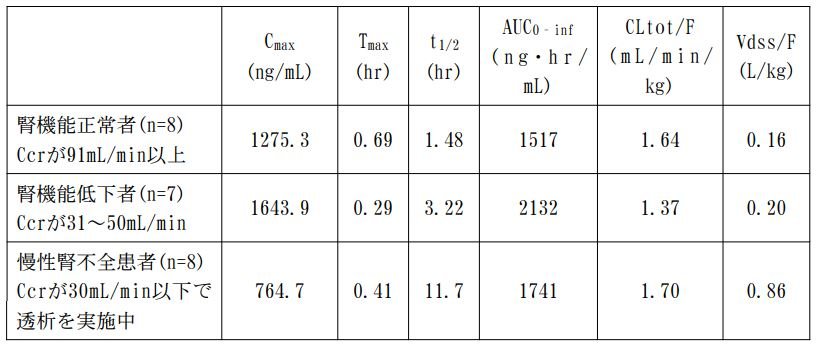
注)グルファスト錠の承認されている用法及び用量は、「通常、成人にはミチグリニドカルシウム水和物として1回10mgを1日3回毎食直前に経口投与する。なお、患者の状態に応じて適宜増減する。」です。
参考資料:
電子添文
インタビューフォーム
〔2025年8月改訂〕-
Q6.グルファスト錠の肝機能障害患者への投与に関する注意事項を教えてください。
肝機能障害患者への投与は、低血糖を起こすおそれや、肝機能障害を悪化させるおそれがあるため、注意が必要です。
ミチグリニドカルシウム水和物は主に肝臓で代謝されるため、肝機能障害のある患者ではミチグリニドカルシウム水和物に対する代謝機能が低下し、低血糖を起こす可能性があります。また、グルファスト錠の単独療法承認時までの臨床試験において、肝機能障害を合併した症例で、肝機能検査値の悪化を認めた例がありました。
なお、α-グルコシダーゼ阻害剤併用投与試験及びチアゾリジン系薬剤併用投与試験においても肝機能障害を合併した症例で、肝機能検査値の悪化を認めた例がありましたが、いずれも軽度でした。参考資料:
電子添文
インタビューフォーム
〔2025年8月作成〕-
Q7.グルファスト錠は高齢者に投与してもよいですか?
高齢者では、状況に応じて低用量(1回量5mg)から投与を開始することが望ましいです。
一般的に高齢者では肝機能や腎機能等の生理機能が低下していることが多く、低血糖等の副作用が発現しやすくなる可能性が考えられるため、高齢者に対しては慎重に投与することが必要です。グルファスト錠10mgの単回経口投与注)における、高齢者(65歳以上)及び非高齢者(20~35歳)の薬物動態パラメータを比較したところ、高齢者群は、非高齢者群に比べCmaxでやや低値を示しましたが、他はほぼ同等の数値でした。また、投与24時間までの尿中排泄率もほぼ同等でした。
なお、グルファスト錠の単独療法承認時の国内臨床試験における副作用発現状況及び臨床検査値異常変動発現状況を、高齢者(65歳以上)と非高齢者(65歳未満)で比較した結果は、以下のとおりです。高齢者と非高齢者における副作用発現状況の比較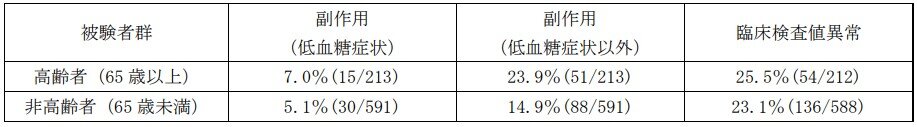
以上のように、高齢者と非高齢者における薬物動態パラメータはほぼ同等でしたが、高齢者において副作用発現率が高頻度にみられることより、低用量(1回量5mg)から投与を開始するなど慎重な投与が必要です。
■高齢者と非高齢者の副作用発現状況の比較(併用投与試験)■
なお、単独療法と副作用の集計方法が異なるため、比較はできませんが、α-グルコシダーゼ阻害剤併用療法時、チアゾリジン系薬剤併用療法時、ビグアナイド系薬剤又はDPP-4阻害剤併用療法時の副作用発現状況は、インタビューフォーム「Ⅷ.安全性(使用上の注意等)に関する項目」に掲載しております。
以下のリンクから、ご参照ください。
注)グルファスト錠の承認されている用法及び用量は、「通常、成人にはミチグリニドカルシウム水和物として1回10mgを1日3回毎食直前に経口投与する。なお、患者の状態に応じて適宜増減する。」です。
参考資料:
電子添文
インタビューフォーム
〔2025年8月作成〕-
Q8.グルファスト錠と併用注意の薬剤を教えてください。
以下の薬剤との併用に注意してください。
※スルホニル尿素系製剤(SU剤)との併用については、「Q4. グルファスト錠はスルホニル尿素系製剤(SU剤)と併用してもよいですか?」をご参照ください。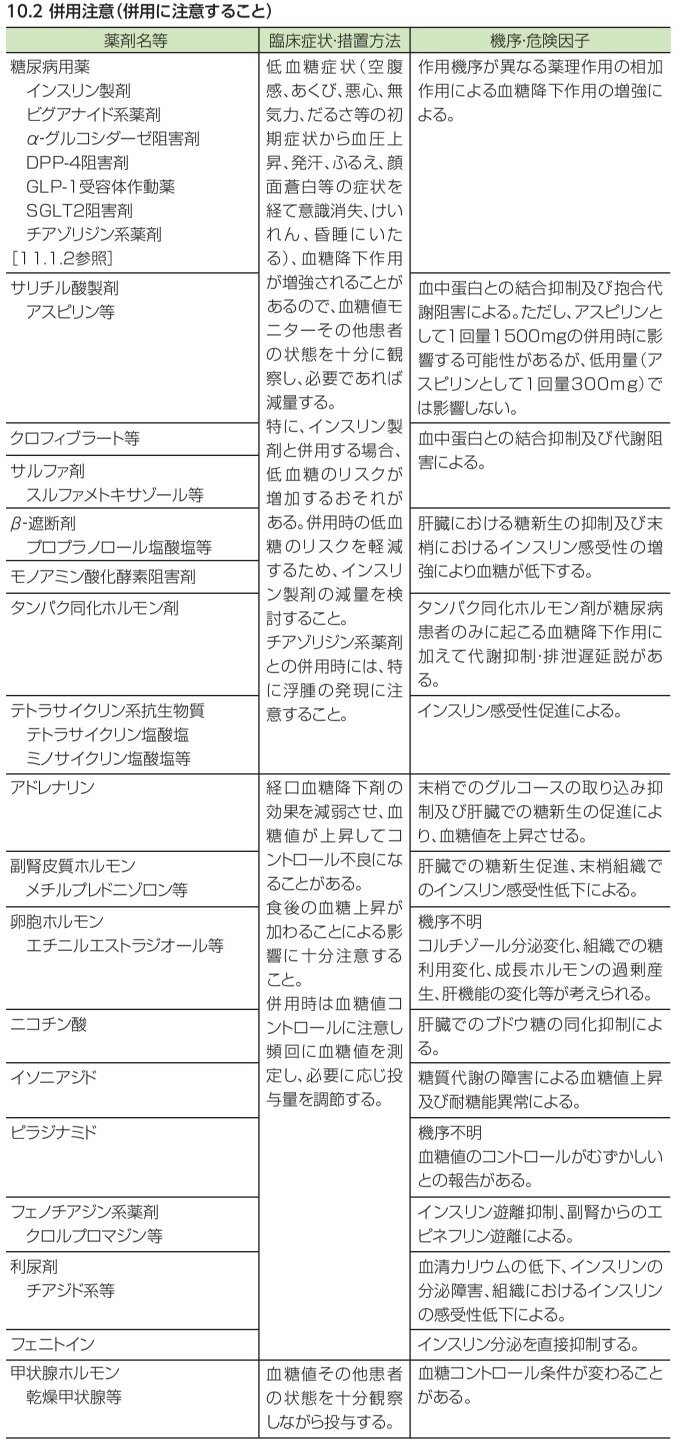
参考資料:
電子添文
〔2025年8月作成〕-
Q9.グルファスト錠の副作用を教えてください。
グルファスト錠の重大な副作用は、心筋梗塞(0.1%)、低血糖(6.6%※)、肝機能障害(頻度不明)です。
※低血糖症状(眩暈、空腹感、振戦、脱力感、冷汗、意識消失等)として報告された発現割合また、その他の副作用は、以下のとおりです。
これらの副作用があらわれることがあるので 、観察を十分に行い、異常が認められた場合には、投与を中止するなど適切な処置を行ってください。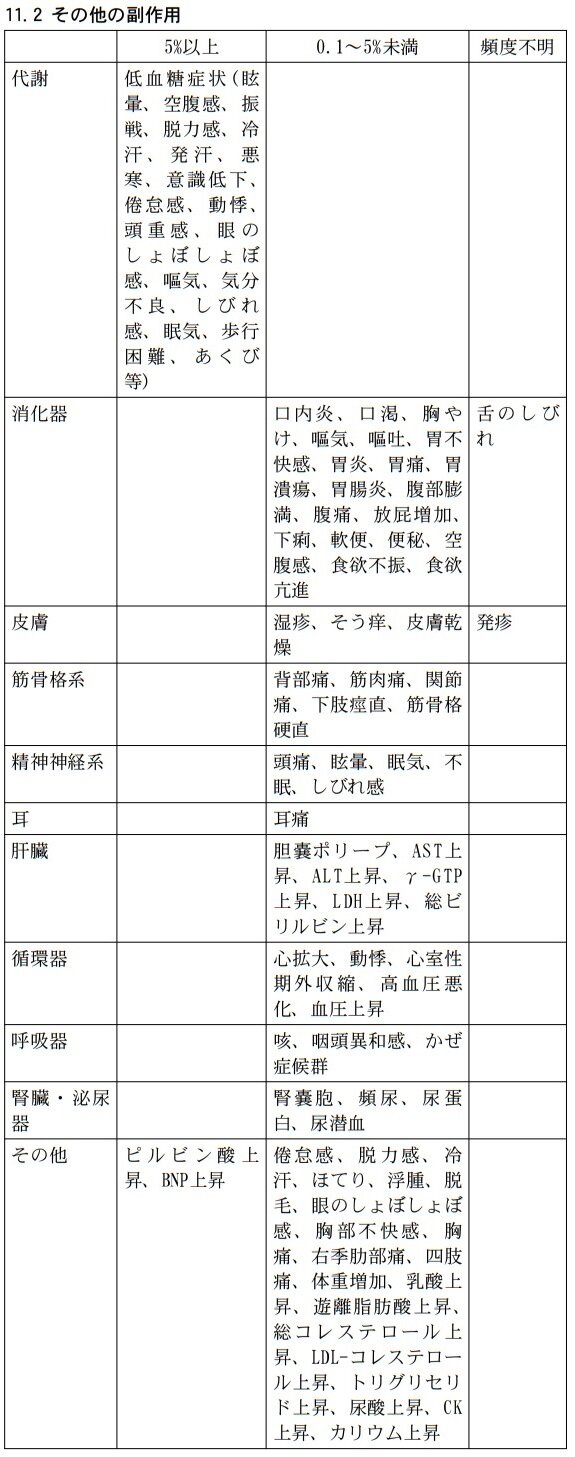
グルファスト錠の臨床試験で認められた副作用は、以下のとおりです。
〇単独療法 第Ⅲ相二重盲検比較試験
食事療法のみでは十分な血糖コントロールが得られない314例の2型糖尿病患者を対象に、グルファスト錠1回10mg又はプラセボを1日3回毎食直前12週間経口投与しました。
副作用(臨床症状)の発現割合は、プラセボ群の22.5%(23/102例)に対し、グルファスト錠群では23.5%(24/102例)でした。
副作用(臨床検査値)の発現割合は、プラセボ群の14.9%(15/101例)に対し、グルファスト群では25.7%(26/101例)でした。
低血糖症状の発現割合は、プラセボ群の2.9%(3/102例)に対し、グルファスト群では2.0%(2/102例)でした。〇単独療法 長期投与試験
2型糖尿病患者351例を対象に、グルファスト錠1回10mg(5mgまたは20mgに増減可能)を1日3回、52週間経口投与しました。
副作用(臨床症状)、副作用(臨床検査値)及び低血糖症状の発現割合は、それぞれ27.5%(98/356例)、22.0%(78/354例)及び9.8%(35/356例)でした。その他の臨床試験における副作用は、電子添文【17. 臨床成績】をご参照ください。
参考資料:
電子添文
インタビューフォーム
〔2025年8月作成〕-
Q10.グルファスト錠の重大な副作用「低血糖」の対処方法を教えてください。
グルファスト錠の投与により、低血糖症状(眩暈、空腹感、振戦、脱力感、冷汗、意識消失等)が認められた場合には、糖質を含む食品を摂取するなど適切な処置を行ってください。ただし、α-グルコシダーゼ阻害剤との併用により低血糖症状が認められた場合には、ブドウ糖を投与してください。
また、1回5mgへの減量を検討するなど慎重に投与してください。参考資料:
電子添文
〔2025年8月改訂〕-
Q11.グルファスト錠とグルファストOD錠で有効性や安全性に違いはありますか?
生物学的同等性試験の結果、グルファスト錠とグルファストOD錠は、生物学的同等性が確認されているため、有効性や安全性は、同等であると考えられます。
健康成人男性にミチグリニドカルシウム水和物10mg(OD錠、水なし又は水で服用)又は、ミチグリニドカルシウム水和物10mg(錠、水で服用)を、空腹時に単回経口投与したとき注)、両製剤は生物学的に同等でした。
注)グルファスト錠・グルファストOD錠の承認されている用法及び用量は、「通常、成人にはミチグリニドカルシウム水和物として1回10mgを1日3回毎食直前に経口投与する。なお、患者の状態に応じて適宜増減する。」です。
参考資料:
電子添文
〔2025年8月改訂〕-
Q12.グルファスト錠の作用機序について教えてください。
ミチグリニドカルシウム水和物は、膵β細胞のスルホニル尿素受容体への結合を介して、ATP感受性K+チャネル(KATPチャネル)電流を阻害することにより、インスリンの分泌を促進します(in vitro)。
以下の作用機序が考えられます。
①ミチグリニドは、膵β細胞のATP感受性K+チャネル(KATPチャネル)を構成するスルホニル尿素受容体(SUR1)に選択的に結合する。 ②ミチグリニドとSUR1との結合によりKATPチャネルが閉鎖される。 ③KATPチャネルの閉鎖により細胞膜が脱分極を起こす。 ④細胞膜の脱分極により電位依存性Ca2+チャネルが開口し、細胞内にCa2+が流入する。 ⑤細胞内のCa2+濃度が上昇してインスリン分泌顆粒を刺激し、インスリンが分泌される。
膵β細胞からのインスリン分泌機構とミチグリニドの作用機序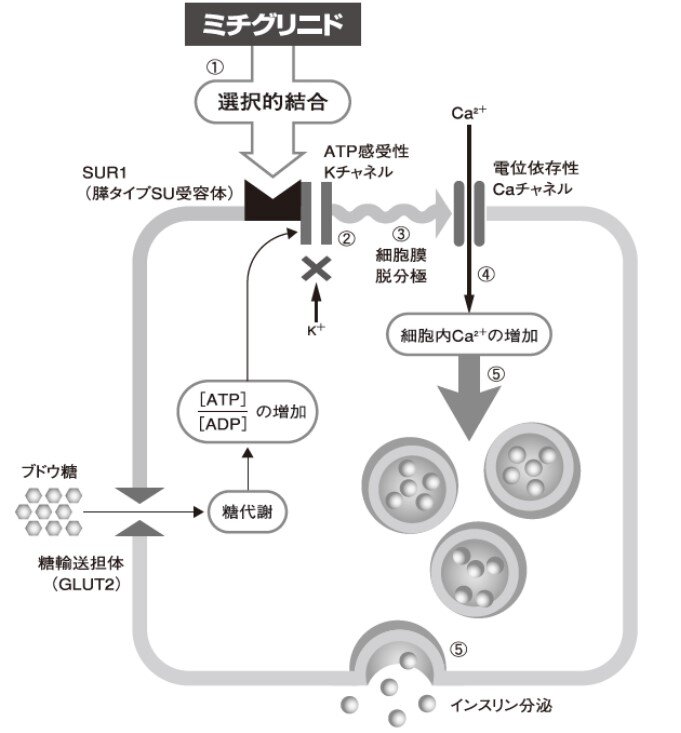
参考資料:
電子添文
インタビューフォーム
〔2025年8月作成〕-
Q13.グルファスト錠の製剤の安定性を教えてください。
グルファスト錠の安定性は、以下のとおりです。
グルファスト錠5mg、10mgの各種条件下における安定性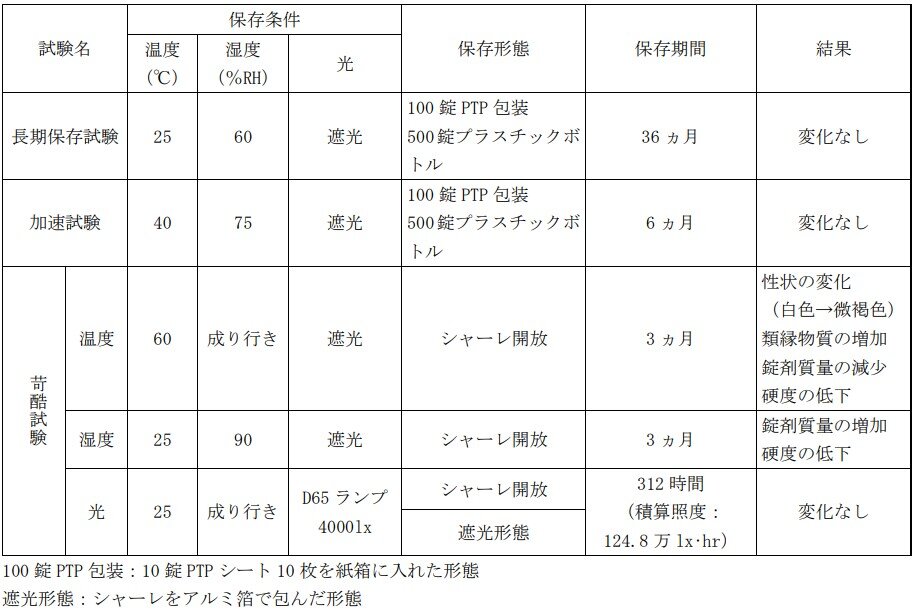
参考資料:
インタビューフォーム
〔2025年8月作成〕-
Q14.グルファスト錠の粉砕、崩壊・懸濁性及び経管チューブの通過性に関する情報を教えてください。
本内容には承認を受けていない品質に関する情報が含まれています。試験方法等が確立していない内容も含まれており、あくまでも記載されている試験方法で得られた結果を事実として提示しています。医療従事者が臨床適用を検討する上での参考情報であり、加工等の可否を示すものではありません。
インタビューフォーム 「XIII.備考」に掲載しております。
以下のリンクから、ご参照ください。■粉砕品の安定性■
■崩壊・懸濁性及び経管チューブの通過性■注:グルファスト錠の承認されている用法及び用量は、「通常、成人にはミチグリニドカルシウム水和物として1回10mgを1日3回毎食直前に経口投与する。なお、患者の状態に応じて適宜増減する。」です。粉砕又は懸濁して投与する方法は、グルファスト錠の承認された用法及び用量ではありません。また、グルファスト錠を粉砕又は懸濁した製品での臨床試験、薬物動態、安定性、有効性及び安全性等のデータはなく、グルファスト錠の粉砕投与及び懸濁投与は推奨しません。
参考資料:
インタビューフォーム
〔2025年8月改訂〕





