イセルティ錠 Q&A
「Q&A」は、医療関係者の皆様に向けて作成しています。
本内容は、製品の適正使用に関する参考情報であり、すべてのケースに当てはまるものではありません。また、国内で承認された効能効果・用法用量の範囲外の情報を含む場合がありますが、当社として推奨するものではありません。製品のご使用にあたっては、最新の電子添文をご確認ください。
「Q&A」のご利用によって、生じた結果につきましては、責任を負いかねますのでご了承ください。
※許可なく複写、複製、転掲、改変等を行うことはご遠慮ください。
-
Q1.「診断のつかない異常性器出血の患者」が、禁忌に設定された理由を教えてください。
診断のつかない異常性器出血の患者は、悪性腫瘍等による出血の可能性があり、イセルティ錠の投与により診断が遅れ悪化するおそれがあるため、禁忌に設定しました。
参考資料:
電子添文
インタビューフォーム
〔2026年3月作成〕-
Q2.イセルティ錠の効能又は効果を教えてください。
イセルティ錠の「効能又は効果」は、以下のとおりです。
子宮筋腫に基づく下記諸症状の改善
過多月経、下腹痛、腰痛、貧血なお、「効能又は効果に関連する注意」は、以下のとおりです。
本剤による治療は根治療法ではないことに留意し、手術が適応となる患者の手術までの保存療法並びに閉経前の保存療法としての適用を原則とすること。参考資料:
電子添文
〔2026年3月作成〕-
Q3.イセルティ錠の用法及び用量を教えてください。
イセルティ錠の用法及び用量は、「通常、成人にはリンザゴリクスとして200mgを1日1回経口投与する。なお、初回投与は月経周期1~5日目に行う。」です。
なお、「用法及び用量に関連する注意」は、以下のとおりです。
7.1 治療に際しては妊娠していないことを確認し、必ず月経周期1~5日目より投与を開始すること。また、治療期間中は非ホルモン性の避妊をさせること。 7.2 エストロゲン低下作用に基づく骨塩量の低下がみられることがあるので、6ヵ月を超える投与は原則として行わないこと。6ヵ月を超える投与の安全性は確立していない。なお、やむを得ず長期にわたる投与や再投与が必要な場合には、可能な限り骨塩量の検査を行い慎重に投与すること。
参考資料:
電子添文
〔2026年3月作成〕-
Q4.イセルティ錠は食事の影響はありますか?
以下の試験結果より、イセルティ錠は、食事の影響を受けません。
食事の影響試験(外国人データ)
閉経前健康女性(22例)を対象にイセルティ錠200mgを高脂肪食摂取後に単回経口投与したとき、空腹時と比較してリンザゴリクスの Cmaxは0.82倍であり、AUC0-∞は1.00 倍でした。AUC0-∞の幾何平均値の比の90%信頼区間は生物学的同等性の範囲内でした。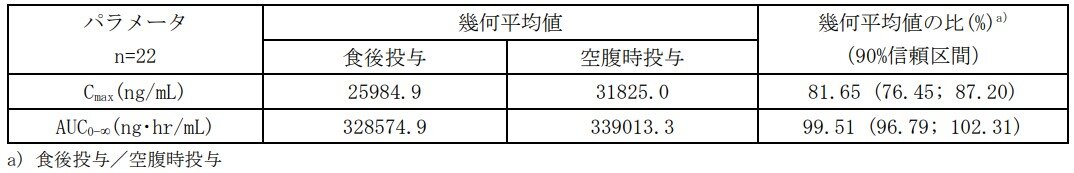
参考資料:
電子添文
インタビューフォーム
〔2026年3月作成〕-
Q5.イセルティ錠を飲み忘れた場合、どうすればよいですか?
飲み忘れた場合は、決して2回分を一度に飲まないでください。気がついた時に、1回分を飲んでください。ただし、次の飲む時間が近い場合は1回とばして、次の時間に1回分飲んでください。
参考資料:
患者向医薬品ガイド
〔2026年3月作成〕-
Q6.イセルティ錠の「QT間隔延長のおそれ又はその既往歴のある患者」への投与に関する注意事項を教えてください。
臨床試験成績より、イセルティ錠の投与によりQT間隔が延長する可能性が示唆されたため、注意が必要です。
国内第Ⅲ相臨床試験(KLH2301及びKLH2302試験)では以下の除外基準を設定しており、当該患者に対する安全性は確認していません。
・臨床的に問題となる心血管疾患(スクリーニング期開始前24週間以内に発現した心筋梗塞、不安定な狭心症など)の合併を有する患者
・Torsades de pointesに対する危険因子の既往歴を有する患者(たとえば、心不全、低カリウム血症、QT延長症候群の家族歴)
<参考>
QT/QTc試験(海外データ)
健康成人女性(48例)を対象として、イセルティ錠200mg、イセルティ錠700mg注)、モキシフロキサシン400mg又はプラセボを単回経口投与したときのQT/QTc間隔に及ぼす影響を評価しました。
イセルティ錠200mg又は700mgを投与したとき、QTcFのベースラインからの変化量のプラセボとの差の最大値は、投与後3時間においてそれぞれ8.34msec(90%信頼区間の上限10.23msec)及び9.92msec(90%信頼区間の上限11.81msec)でした。イセルティ錠200mg及び700mgはQT間隔を延長する可能性が示唆されました。
カテゴリカル解析の結果、イセルティ錠200mg及び700mgのいずれも、投与後のQTcF間隔はすべての時点で480msec以下であり、ベースラインからの変化量はすべての時点で30msec以下でした。
注)イセルティ錠の承認されている用法及び用量は、「通常、成人にはリンザゴリクスとして200mgを1日1回経口投与する。なお、初回投与は月経周期1~5日目に行う。」です。参考資料:
電子添文
インタビューフォーム
〔2026年3月作成〕-
Q7.イセルティ錠の「粘膜下筋腫のある患者」への投与に関する注意事項を教えてください。
粘膜下筋腫のある患者では、観察を十分に行い、異常が認められた場合には適切な処置を行ってください。また、一度に大量の出血が認められた場合には、速やかに医療機関に連絡するよう患者を指導してください。筋腫分娩、重度の不正出血があらわれることがあります。
参考資料:
電子添文
インタビューフォーム
〔2026年3月作成〕-
Q8.イセルティ錠の腎機能障害患者への投与に関する注意事項を教えてください。
重度の腎障害のある患者及び末期腎不全患者では、イセルティ錠の減量を考慮するとともに、患者の状態を慎重に観察し、副作用の発現に十分注意してください。非結合形リンザゴリクスの血中濃度が上昇し、副作用が強くあらわれるおそれがあります。
中等度の腎障害のある患者では、非結合形リンザゴリクスの血中濃度が上昇し、副作用が強くあらわれるおそれがあります。
軽度、中等度及び重度の腎機能障害患者、血液透析を要する末期腎不全患者、並びに腎機能正常被験者にイセルティ錠200mgを単回経口投与したとき、腎機能障害の程度がリンザゴリクスの薬物動態に及ぼす影響は以下のとおりでした(外国人データ)。
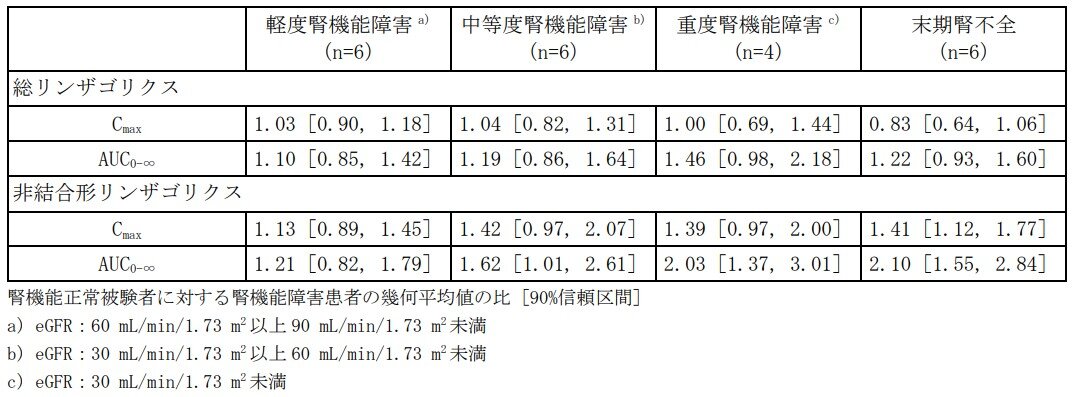
参考資料:
電子添文
〔2026年3月作成〕-
Q9.イセルティ錠の肝機能障害患者への投与に関する注意事項を教えてください。
重度(Child-Pugh分類C)の肝障害のある患者では、イセルティ錠を減量するとともに、患者の状態を慎重に観察し、副作用の発現に十分注意してください。非結合形リンザゴリクスの血中濃度が上昇し、副作用が強くあらわれるおそれがあります。
軽度、中等度及び重度の肝機能障害患者並びに肝機能正常被験者にイセルティ錠200mgを単回経口投与したとき、肝機能障害の程度がリンザゴリクスの薬物動態に及ぼす影響は以下のとおりでした(外国人データ)。
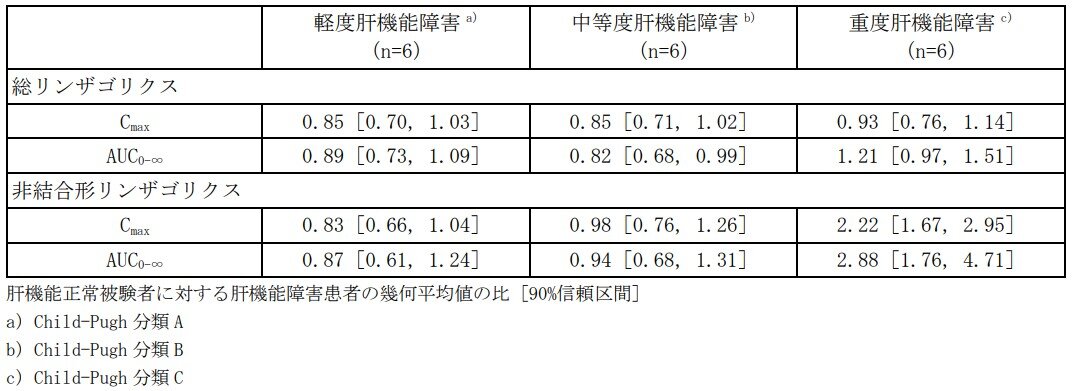
参考資料:
電子添文
〔2026年3月作成〕-
Q10.イセルティ錠は妊婦に投与しても良いですか?
妊婦又は妊娠している可能性のある女性には、投与しないでください。
動物試験で全胚死亡(ラット)及び不妊(ウサギ)が認められています。また、動物試験(ラット)でリンザゴリクスの胎盤通過性が認められています。<参考(ラット)>
妊娠13日目及び17日目の絶食した妊娠ラットに[14C]リンザゴリクスコリン(3mg/kg)を単回経口投与したとき、母動物の多くの組織中放射能濃度は投与後2時間に最高値を示し、血漿中放射能濃度と同様に低下しました。
妊娠13日目のラットでは、投与後8時間から胎児組織中に放射能が検出され、投与後72時間及び168時間に最高濃度に達しました。
妊娠17日目のラットでは、投与後2時間から胎児の血液、脳、肝臓、腎臓及び全身の放射能濃度が上昇し、投与後48時間又は72時間に最高濃度に達しました。
投与後2~24時間の胎児組織中放射能濃度は、母動物の血漿中濃度よりも低値でした。投与後72時間においては、胎児の血液、腎臓及び全身の放射能濃度は母動物の血漿よりも高値でした。胎児1匹あたりに分布した放射能は、いずれの時点においても投与量の1%未満でした。
胎児組織中の放射能は母動物に比べ緩やかに上昇したことから、リンザゴリクス及びその代謝物は胎盤を通過し、緩やかに胎児に分布すると考えられました。参考資料:
電子添文
インタビューフォーム
〔2026年3月作成〕-
Q11.イセルティ錠は授乳婦に投与しても良いですか?
授乳婦に投与する場合、授乳を避けさせてください。また、授乳管理ができない方には投与しないで下さい。
動物試験(ラット)でリンザゴリクスの乳汁移行が認められており、性腺刺激ホルモンの分泌抑制作用により乳児の生殖機能等の成熟に影響を及ぼすおそれがあります。<参考(ラット)>
哺育ラット(分娩後8~9日目)に[14C]リンザゴリクスコリン(3mg/kg)を単回経口投与し、母動物の血漿及び乳汁中放射能濃度を測定しました。
乳汁中放射能濃度は投与後13.3時間にCmax(1315.66ng eq./mL)に達し、22.8時間のt1/2で低下しました。乳汁中放射能濃度はいずれの時点においても血漿中放射能濃度より低く(<0.3倍)、乳汁中放射能のAUC0-∞は血漿の約0.2倍でした。リンザゴリクス及びその代謝物は乳汁中に緩やかに移行しましたが、移行性は低いと考えられました。参考資料:
電子添文
インタビューフォーム
〔2026年3月作成〕-
Q12.イセルティ錠と併用注意の薬剤を教えてください。
リンザゴリクスは、CYP2C8に対する弱い阻害作用を有します。
以下の薬剤との併用に注意してください。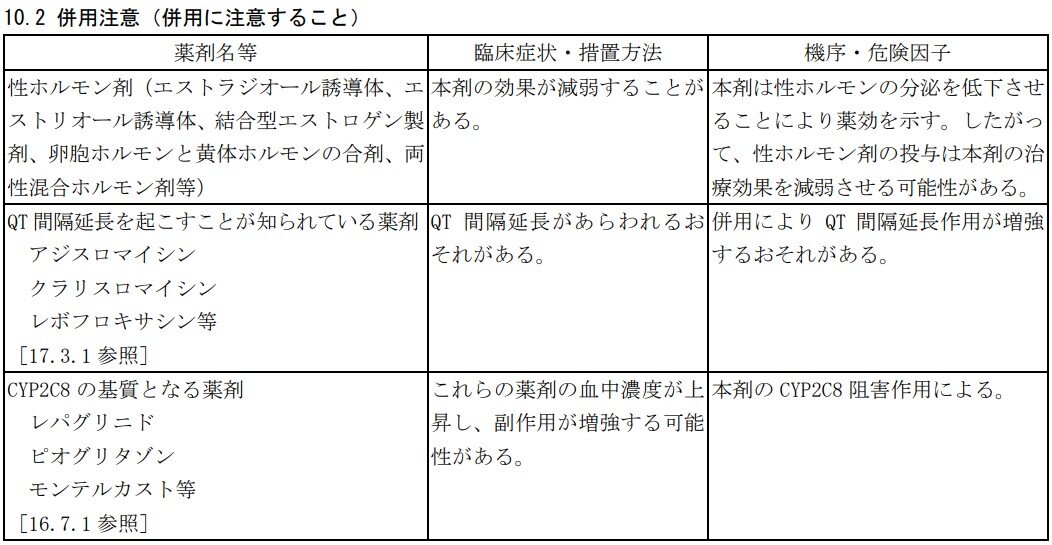
参考資料:
電子添文
〔2026年3月作成〕-
Q13.イセルティ錠の副作用について教えてください。
イセルティ錠の重大な副作用は、うつ状態(1%未満)です。
エストロゲン低下作用に基づく更年期障害様のうつ状態があらわれることがあります。また、その他の副作用は、以下のとおりです。
これらの副作用があらわれることがあるので、医師の指導の下、観察を十分に行い、異常が認められた場合には、投与を中止するなど適切な処置を行ってください。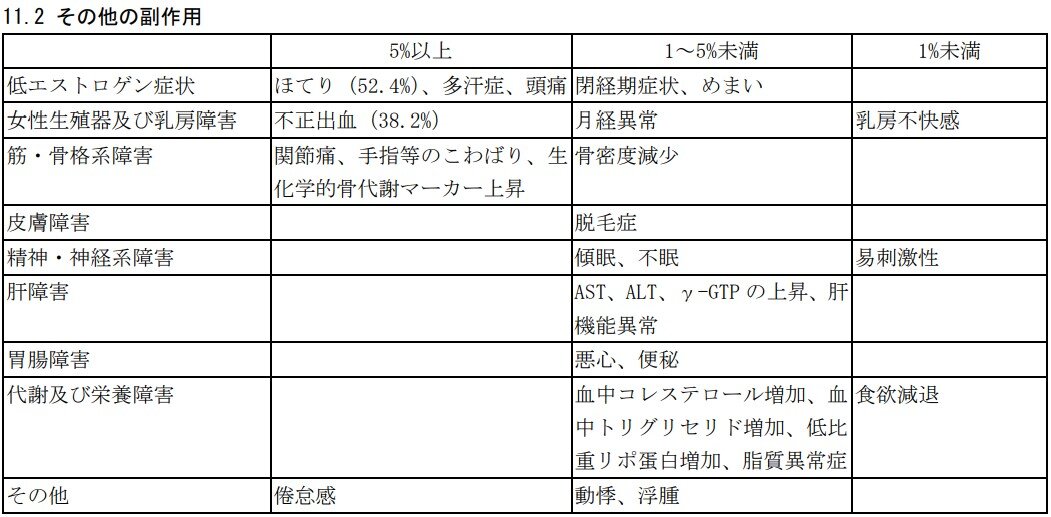
参考資料:
電子添文
〔2026年3月作成〕-
Q14.イセルティ錠の重大な副作用「うつ状態」について教えてください。
臨床試験成績より、エストロゲンの低下作用に基づく更年期障害様のうつ状態が認められています。うつ状態に関連する重篤な有害事象は認められなかったものの、うつ状態は重症化した場合に重大な転帰※につながるおそれがあることから、注意が必要です。
※重大な転帰:自殺未遂、自殺念慮や自傷等参考資料:
電子添文
インタビューフォーム
〔2026年3月作成〕-
Q15.イセルティ錠の医薬品リスク管理計画書(RMP)及び関連資料はありますか?
イセルティ錠のRMPは、以下のリンクからご参照ください。
■イセルティ錠100mgに係る医薬品リスク管理計画書(RMP)■
なお、イセルティ錠には、医療従事者向け及び患者さん向けRMP資材はありません。
参考資料:
イセルティ錠100mgに係る医薬品リスク管理計画書(RMP)
〔2026年3月作成〕-
Q16.イセルティ錠の代謝について教えてください。
ヒト肝ミクロソーム及びヒトCYP発現ミクロソームを用いた試験において、リンザゴリクスは主にCYP2C9、CYP2C8及びCYP3A4により代謝されました(in vitro)。
<参考>(in vitro)
・CYP誘導作用
リンザゴリクスはヒト肝細胞においてCYP1A2及び2B6を誘導しないこと、並びに150μmol/LではCYP3A4/5に対する誘導能を有することが示唆されました。
・CYP阻害作用
リンザゴリクスは、CYP2C8活性に対して可逆的阻害作用(IC50:2.89μmol/L)及び時間依存的阻害作用(KI:3.34μmol/L、kinact:0.00639min-1)を示しました。参考資料:
電子添文
インタビューフォーム
〔2026年3月作成〕-
Q17.イセルティ錠の排泄について教えてください。
閉経後健康女性6例に[14C]リンザゴリクス200mgを単回経口投与したとき、放射能の尿中及び糞中への排泄率は、それぞれ投与量の51.5%及び38.4%でした。リンザゴリクス(未変化体)の尿中及び糞中への排泄率は、それぞれ投与量の20.6%及び4.9%でした(外国人データ)。
参考資料:
電子添文
〔2026年3月作成〕-
Q18.イセルティ錠の作用機序について教えてください。
リンザゴリクスは下垂体前葉に発現しているGnRH受容体に対して選択的な拮抗作用を示し、GnRHの作用を遮断します。それにより、下垂体からの性腺刺激ホルモン(LH及びFSH)分泌を阻害し、卵巣からの性ホルモン(E2、プロゲステロン等)分泌を阻害します。
リンザゴリクスは卵巣におけるE2の一時的な産生増加(フレアアップ)を起こすことなく、子宮筋腫の症状を改善すると考えられます。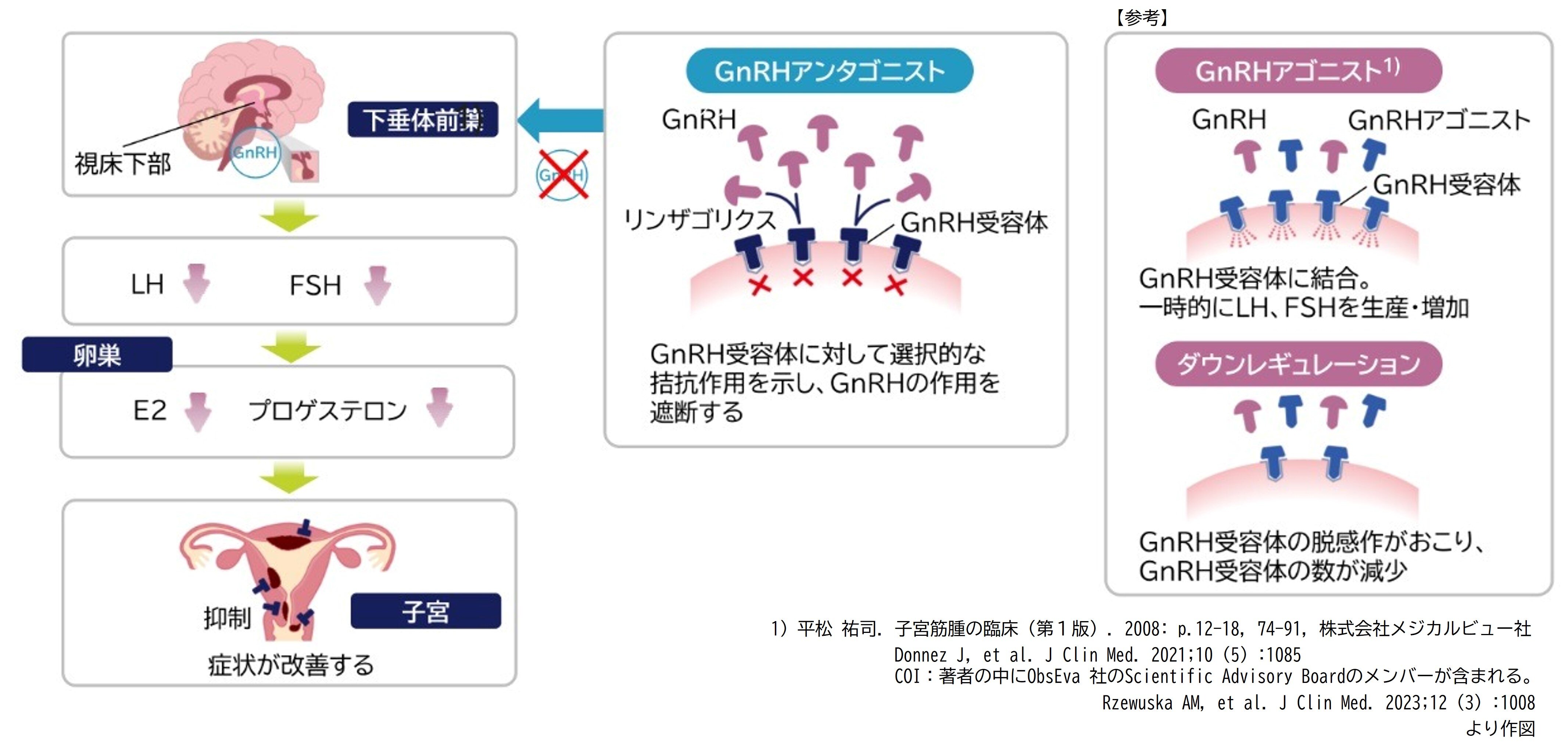
参考資料:
電子添文
インタビューフォーム
〔2026年3月作成〕-
Q19.イセルティ錠の製剤の安定性を教えてください。
イセルティ錠の安定性は、以下のとおりです。
1)イセルティ錠100mgの各種条件下における安定性
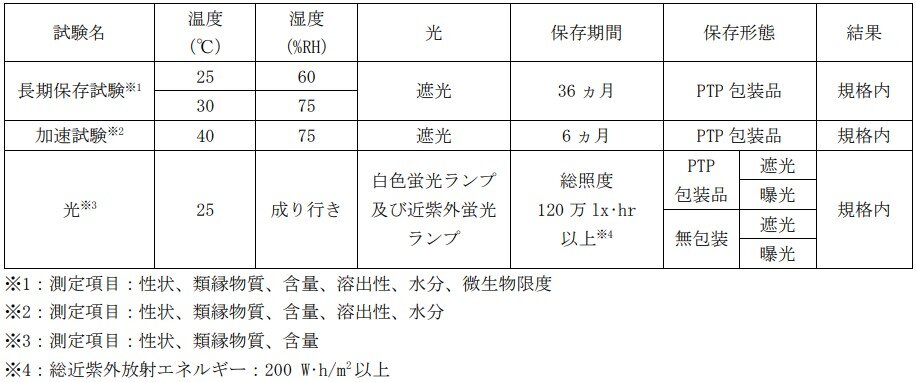
2)イセルティ錠100mgの無包装の安定性
「錠剤・カプセル剤の無包装状態での安定性試験法について(答申)(日本病院薬剤師会)(平成11年8月20日付)」の評価方法に準じた安定性情報を以下に示す。
参考資料:
インタビューフォーム
〔2026年3月作成〕-
Q20.イセルティ錠の海外での承認・発売状況を教えてください。
イセルティ錠は、2022年6月に欧州及び英国において子宮筋腫に係る効能・効果で承認されて以降、2025年9月現在、子宮筋腫に係る効能・効果で30以上の国又は地域において承認されています。
なお、本邦における効能又は効果、用法及び用量は、海外での承認状況とは異なります。イセルティ錠の電子添文に記載されている承認内容の範囲で、イセルティ錠を使用してください。
参考資料:
インタビューフォーム
審査報告書
〔2026年3月作成〕-
Q21.イセルティ錠の粉砕、崩壊・懸濁性及び経管チューブの通過性に関する情報を教えてください。
本内容には承認を受けていない品質に関する情報が含まれています。試験方法等が確立していない内容も含まれており、あくまでも記載されている試験方法で得られた結果を事実として提示しています。医療従事者が臨床適用を検討する上での参考情報であり、加工等の可否を示すものではありません。
インタビューフォーム XIII.備考「1.調剤・服薬支援に際して臨床判断を行うにあたっての参考情報」に掲載しております。
以下のリンクから、ご参照ください。注:イセルティ錠の承認されている用法及び用量は、「通常、成人にはリンザゴリクスとして200mgを1日1回経口投与する。なお、初回投与は月経周期1~5日目に行う。」です。粉砕又は懸濁して投与する方法は、イセルティ錠の承認された用法及び用量ではありません。また、イセルティ錠を粉砕又は懸濁した製品での臨床試験、薬物動態、安定性、有効性及び安全性等のデータはなく、イセルティ錠の粉砕投与及び懸濁投与は推奨しません。
参考資料:
インタビューフォーム
〔2026年3月作成〕




